题目内容
甲酸甲酯水解反应方程式为:HCOOCH3 + H2O  HCOOH + CH3OH – Q(Q>0)
HCOOH + CH3OH – Q(Q>0)
某小组通过实验研究该反应(反应过程中体积变化忽略不计)。反应体系中各组分的起始量如下表。甲酸甲酯转化率在温度T1下随反应时间(t)的变化如下图:

(1)上述反应的平衡常数表达式为K=_______________________。
(2)计算15~20min范围内:甲酸甲酯的减少量为 mol,甲酸甲酯的平均反应速率为 mol/min;80~90min范围内甲酸甲酯的平均反应速率为___________ mol/min。
(3)依据以上数据,推断该反应在10min后反应速率迅速加快的原因: 。
(4)其他条件不变,提高温度为T2,在答题卡框图中画出温度T2下甲酸甲酯转化率随反应时间变化的预期结果示意图。
 HCOOH + CH3OH – Q(Q>0)
HCOOH + CH3OH – Q(Q>0)某小组通过实验研究该反应(反应过程中体积变化忽略不计)。反应体系中各组分的起始量如下表。甲酸甲酯转化率在温度T1下随反应时间(t)的变化如下图:
| 组分 | 物质的量/mol |
| HCOOCH3 | 1.00 |
| H2O | 1.99 |
| HCOOH | 0.01 |
| CH3OH | 0.52 |

(1)上述反应的平衡常数表达式为K=_______________________。
(2)计算15~20min范围内:甲酸甲酯的减少量为 mol,甲酸甲酯的平均反应速率为 mol/min;80~90min范围内甲酸甲酯的平均反应速率为___________ mol/min。
(3)依据以上数据,推断该反应在10min后反应速率迅速加快的原因: 。
(4)其他条件不变,提高温度为T2,在答题卡框图中画出温度T2下甲酸甲酯转化率随反应时间变化的预期结果示意图。
(1) (1分)
(1分)
(2)0.045 , 9.0×10-3, 0(3分)
(3)该反应中甲酸具有催化作用,甲酸量逐渐增多,催化效果显著,反应速率明显增大。(2分)
(4) (2分)
(2分)
 (1分)
(1分)(2)0.045 , 9.0×10-3, 0(3分)
(3)该反应中甲酸具有催化作用,甲酸量逐渐增多,催化效果显著,反应速率明显增大。(2分)
(4)
 (2分)
(2分)试题分析:
(1)化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据反应的化学方程式可知,平衡常数
 。
。(2)根据图中的转化率可知,15min时甲酸甲酯的转化率是6.7%,则消耗甲酸甲酯的物质的量是0.067mol。20min时甲酸甲酯的转化率是11.2%,则消耗甲酸甲酯的物质的量是0.112mol,所以在15~20min内甲酸甲酯减少了0.112mol-0.067mol=0.045。则甲酸甲酯的平均反应速率为0.045mol÷5min=0.009mol/min;根据图像可知,80min后反应物的转化率不再发生变化,说明反应已经达到平衡状态,则80~90min范围内甲酸甲酯的平均反应速率为0。
(3)由于在该反应中甲酸具有催化作用,随着反应的进行,甲酸量逐渐增多,催化效果显著,反应速率明显增大。
(4)正反应是吸热反应,所以升高温度,反应物的转化率增大。且反应速率快,达到平衡的时间少,即图像是(见答案)。

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
 pC(g)+ qD(g);根据下图示回答:
pC(g)+ qD(g);根据下图示回答: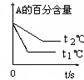
 CH3OCH3(g)+H2O(g)。某温度下的平衡常数为400。此温度下,在体积恒定的密闭容器中加入一定量的CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)。某温度下的平衡常数为400。此温度下,在体积恒定的密闭容器中加入一定量的CH3OH,反应到某时刻测得各组分的浓度如下: 2SO3(g) ΔH<0。下列有关叙述正确的是
2SO3(g) ΔH<0。下列有关叙述正确的是 2NH3(g) △H=-92kJ/mol,若只改变下列一个条件,一定能增大正反应速率且使平衡向正反应方向移动的是( )
2NH3(g) △H=-92kJ/mol,若只改变下列一个条件,一定能增大正反应速率且使平衡向正反应方向移动的是( )
 4NH3 (g)+3O2 (g)+ Q
4NH3 (g)+3O2 (g)+ Q 
 Si (s)+ 4HCl(g) -236kJ
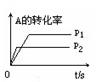
Si (s)+ 4HCl(g) -236kJ 4NO2(g)+ O2(g) △H﹥0。反应物和部分生成物的物质的量随反应时间变化的曲线如图所示,下列说法正确的是
4NO2(g)+ O2(g) △H﹥0。反应物和部分生成物的物质的量随反应时间变化的曲线如图所示,下列说法正确的是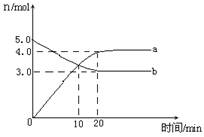
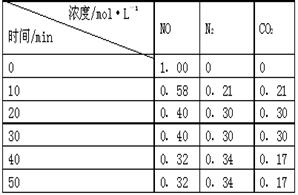
 N2(g)+CO2(g) 。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如右表:
N2(g)+CO2(g) 。某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如右表: