题目内容
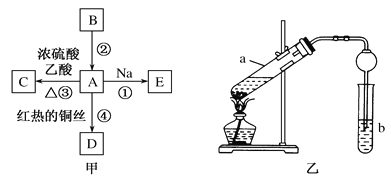
【题目】A、B、C、D为短周期主族元素,25℃时,其最高价氧化物的水化物溶液(浓度均为0.1mol·L-1) 的pH和原子序数的关系如图所示。下列有关说法正确的是

A. 简单离子半径:D离子>C离子>A离子>B离子
B. D元素氧化物的水化物一定是强酸
C. B、C的简单离子都能破坏水的电离平衡
D. 氢化物还原性:C >D
【答案】D
【解析】由题意A、B、C、D是短周期主族元素且原子序数依次增大,最高价氧化物对应的水化物(浓度均为0.1mol/L)溶液的pH,B对应pH=13,说明B是钠,A对应pH=1,A是氮,C对应pH<1,所以C是硫,D对应pH=1,所以D是Cl。A. 一般而言,电子层数越多,离子半径越大,电子层数相同时,核电荷数越大,离子半径越小,简单离子半径:C离子>D离子> A离子>B离子,故A错误;B. 次氯酸是弱酸,故B错误;C. 钠离子不水解,不都能破坏水的电离平衡,故C错误;D. 元素的非金属性越弱,氢化物还原性越强,非金属性:C <D,则还原性:,故D正确;故选D。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案【题目】为完成相应实验,实验器材(规格和数量不限)足够的一项是
相应实验 | 实验器材(省略夹持装置) | |
A | 氯化钠溶液的浓缩结晶 | 烧杯、玻璃棒、酒精灯 |
B | 用盐酸除去硫酸钡中的少量碳酸钡 | 烧杯、漏斗、胶头滴管、滤纸 |
C | 用浓硫酸配制0.5mol·L-1的溶液 | 烧杯、玻璃棒、胶头滴管、容量瓶 |
D | 用溴水和CCl4除去NaBr溶液中的少量NaI | 烧杯、玻璃棒、胶头滴管、分液漏斗 |
A. A B. B C. C D. D
【题目】汽车尾气是导致雾霾天气的重要源头之一,其含有的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应。
(一)已知:反应l: N2(g)+O2(g)=2NO(g) △H1 K1
反应2: CO(g)+ 1/2O2(g)=CO2 (g) △H2 K2
反应3: 2NO(g)+2C0(g)=N2(g)+CO2(g) △H3 K3
则反应3的焓变△H3=_______(用△H1和△H2表示) 平衡常数K3=_____(用K1和K2表示)。
(二)向1.0L恒容密闭容器中,充入N2O(g)和C0(g),可发生如下反应:
N2O(g)+C0(g) ![]() N2(g)+CO2(g),所得实验数据如下表:
N2(g)+CO2(g),所得实验数据如下表:
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(N2O) | n(CO) | n(CO2) | ||
① | 400 | 0.20 | 0.30 | 0.14 |
② | 500 | 0.10 | 0.40 | 0.080 |
③ | 500 | 0.30 | 0.20 | A |
④ | 600 | 0.60 | 0.40 | B |
上述实验编号①中,若10min时测得n(N2)=0.12mol,则0至10min内,用CO2表示的平均反应速率以v(CO2)=________;
(2)500℃时,欲使N2O的平衡转化率a(N2O)≥80%,则起始时n(N2O):n(CO)≤______。
(3)上述实验编号④达平衡时,b____0.24(填“>”、“<”或“=”),原因是_______。
(4) N2O(g)+C0(g)![]() N2(g)+CO2(g)的反应体系达到平衡后,各物质的浓度在不同条件下的变化情况如下图所示:
N2(g)+CO2(g)的反应体系达到平衡后,各物质的浓度在不同条件下的变化情况如下图所示:
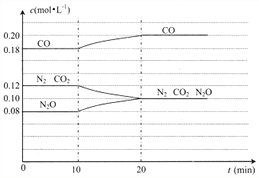
①若在第10min仅改变了一个条件,第20min时是在条件下达到新的平衡状态,则第10min 时改变的条件可能是_______;
②比较CO在第5min和第25min时速率的大小v(5)____v(25)(填”>”、“<”或“= ”),你判断的理由是______________。