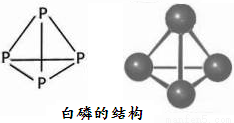
题目内容
在101kPa和25℃时,有关反应的热化学方程式如下:
C(s)+O2(g)=CO2(g)ΔH1=-394kJ·mol-1
C(s)+1/2O2(g)=CO(g)ΔH2=-111kJ·mol-1
2H2(g)+O2(g)=2H2O(g)ΔH3=-484kJ·mol-1
在相同条件下,H2(g)+CO2(g)=CO(g)+H2O(g)ΔH,则ΔH是
A.+41kJ·mol-1
B.-41kJ·mol-1
C.-152kJ·mol-1
D.-263kJ·mol-1
碳和氮是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,目前,这些有毒有害气体的处理成为科学研究的重要内容。
(1)已知2.00g的C2H2完全燃烧生成液态水和二氧化碳气体放出99.6kJ热量,写出表示C2H2燃烧热的热化学方程式。
(2)利用上述反应设计燃料电池(电解质溶液为氢氧化钾溶液),写出电池负极的电极反应式。
(3)用活性炭还原法处理氮氧化物,有关反应为:C(s)+2NO(g) N2(g)+CO2(g)。某研究小组向一个容器容积为3L且容积不变的密闭真空
N2(g)+CO2(g)。某研究小组向一个容器容积为3L且容积不变的密闭真空 容器(固体试样体积忽略不计)中加入NO和足量的活性炭,在恒温(T1℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表:
容器(固体试样体积忽略不计)中加入NO和足量的活性炭,在恒温(T1℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表:
物质 n/mol t/min | NO | N2 | CO2 |
0 | 2.00 | 0 | 0 |
10 | 1.16 | 0.42 | 0.42 |
20 | 0.80 | 0.60 | 0.60 |
30 | 0.80 | 0.60 | 0.60 |
①10min~20min以v(NO)表示的反应速率为。
②下列各项能判断该反应达到平衡状态的是(填序号字母)。
A.v(NO)(正)=2v(N2)(逆)B.容器内CO2和N2的体积比为1:1
C.混合气体的平均相对分子质量保持不变D.容器内压强保持不变
E.混合气体的密度保持不变
③一定温度下,随着NO的起始浓度增大,则NO的平衡转化率(填“增大”、“不变”或“减小”)。
(4)在3L容积可变的密闭容器中发生上述反应:H2(g)+CO2(g) H2O(g)+CO(g),恒温下c(CO)随反应时间t变化的曲线Ⅰ如下图所示。
H2O(g)+CO(g),恒温下c(CO)随反应时间t变化的曲线Ⅰ如下图所示。

①若在t0时改变一个条件,使曲线Ⅰ变成曲线Ⅱ,则改变的条件是________;
②若在t0时刻将容器体积快速压缩至2L(其他条件不变),请在下图中画出c(CO)随反应时间t变化的曲线。

(5)已知:CO(g)+H2O(g) H2(g)+CO2(g)△H=-41.2kJ/mol,850℃时在一体积为10L的恒容密闭容器中,通入一定量的CO和H2O,CO和H2O浓度变化如右图所示:下列说法正确的是(填序号)
H2(g)+CO2(g)△H=-41.2kJ/mol,850℃时在一体积为10L的恒容密闭容器中,通入一定量的CO和H2O,CO和H2O浓度变化如右图所示:下列说法正确的是(填序号)
A.达到平衡时,氢气的物质的量是0.12mol
B.达到平衡时,反应体系最终会放出49.44kJ热量
C.第6min时,若升高温度,反应正向移动
D.第8min时,若充入氦气,会导致v正(CO)<v逆(H2O)
(6)下图表示在温度分别为T1、T2时,平衡体系中CO的体积分数随压强变化曲线,A、C两点的反应速率AC(填“>”、“=”或“<”,下同),由状态B到状态A,可采用的方法(填“升温”或“降温”)。


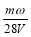 mol·L-1 B.
mol·L-1 B.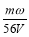 mol·L-1 C.
mol·L-1 C. mol·L-1 D.
mol·L-1 D.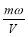 mol·L-1
mol·L-1