题目内容
【题目】据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,其负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。下列说法正确的是
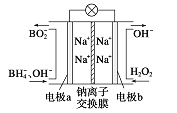
A. 该电池的负极反应为BH4-+8OH--8e-=BO2-+6H2O
B. 电池放电时Na+从b极区移向a极区
C. 每消耗3 mol H2O2,转移的电子为3 mol
D. 电极a采用MnO2作电极材料
【答案】A
【解析】
A.BH4-被氧化为BO2-,应为原电池的负极反应,电极反应式为BH4-+8OH--8e-=BO2-+6H2O,A正确;
B.BH4-被氧化为BO2-,应为原电池的负极反应,正极H2O2得电子被还原生成OH-,原电池工作时,阳离子向正极移动,则电池放电时Na+从a极区移向b极区,B错误;
C.每消耗3molH2O2,转移的电子为6mol,C错误;
D.电极a为原电池的负极,电极材料采用Pt/C,D错误;
答案选A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目