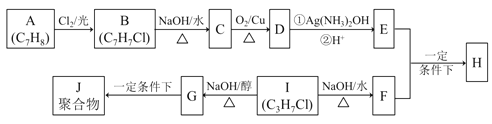
题目内容
【题目】Ⅰ已知NiXO晶体晶胞结构为NaCl型(如图),由于晶体缺陷,x值小于1。测知NiXO晶体x=0.88,晶胞边长为4.28×10-10m 求:(已知:![]() =1.4)
=1.4)
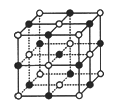
(1)晶胞中两个Ni原子之间的最短距离___________m(精确至0.01)。
(2)与O2-距离最近且等距离的Ni离子围成的几何体形状___ ____。
(3)晶体中的Ni分别为Ni2﹢、Ni3﹢,求此晶体的化学式_________。
(4)已知,NiO晶体熔点大于NaCl,主要原因是______________________________。
Ⅱ金晶体是面心立方最密堆积,立方体的每个面上5个金原子紧密堆砌(如图,其余各面省略),金原子半径为A cm,求:
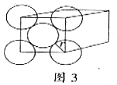
(1)金的密度为___________![]() 。(用带A计算式表示)
。(用带A计算式表示)
(2)金原子空间占有率为___________。(用带A计算式表示)
【答案】
Ⅰ(1) 3.00x10-10m
(2)正八面体
(3)Ni0.64Ni0.24O
(4)Ni2+ 、O2-电荷多,晶格能大
Ⅱ(1)![]()
(2) 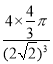
【解析】
试题分析:Ⅰ、(1)由于NiXO晶体晶胞结构为NaCl型,所以晶胞中两个Ni原子之间的最短距离为晶胞面对角线的1/2,由晶胞棱边长可得晶胞面对角线为长为:![]() a,则晶胞中两个Ni原子之间的最短距离为:
a,则晶胞中两个Ni原子之间的最短距离为:![]() a=
a=![]() ×4.28×10-10m=3.00x10-10m;
×4.28×10-10m=3.00x10-10m;
(2)根据晶胞结构可知与O2-距离最近且等距离的Ni离子围成的几何体形状为正八面体;
(3)设晶体中Ni2﹢与Ni3﹢的个数分别为x:y,根据NiXO中化合价代数和为零可知2x+3y=2、x+y=0.88,解得x=0.64、y=0.24,则化学式为Ni0.64Ni0.24O;
(4)由于Ni2+ 、O2-电荷多,晶格能大,所以NiO晶体熔点大于NaCl。
Ⅱ、(1)根据面心立方最密堆积的晶胞可知晶胞含有金原子的个数是![]() ,金原子半径为A cm,则面对角线是4Acm,因此晶胞的边长是
,金原子半径为A cm,则面对角线是4Acm,因此晶胞的边长是![]() ,晶胞的体积为
,晶胞的体积为![]() ,所以金的密度为
,所以金的密度为![]() 。
。
(2)金原子空间占有率为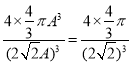 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:
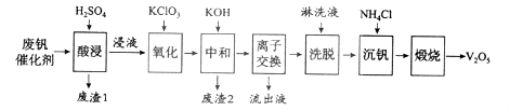
回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________,同时V2O4转成VO2+。“废渣1”的主要成分是__________________。
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为______mol。
(3)“中和”作用之一是使钒以V4O124形式存在于溶液中。“废渣2”中含有_______。
(4)“离子交换”和“洗脱”可简单表示为:4ROH+ V4O124![]() R4V4O12+4OH(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”、“碱”或“中”)。
R4V4O12+4OH(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”、“碱”或“中”)。
(5)“流出液”中阳离子最多的是________。
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________。