题目内容
4.实验室制备、收集干燥的SO2,所需仪器如图.
(1)装置A产生SO2,按气流方向连接各仪器接口,顺序为a→d→e→c→bf.
(2)验证产生的气体是SO2的方法是将气体通入品红溶液中,如果品红褪色,加热后又恢复红色.
分析 (1)利用实验仪器的连接,铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水;安全瓶的使用以及尾气吸收来分析;
(2)二氧化硫的验证,利用其特殊性质漂白性来分析.
解答 解:(1)收集二氧化硫应先干燥再收集,故先通过d、e,二氧化硫的密度比空气大,要从c口进气,b口出来进行尾气处理.因为二氧化硫易于氢氧化钠反应,故f的作用是安全瓶,防止倒吸;盛放NaOH溶液的烧杯为尾气处理装置要放置在最后,按气流方向连接各仪器接口,顺序为a→d→e→c→b→f,
故答案为:d;e;c;b;
(2)检验二氧化硫的一般方法是将气体通入品红溶液中,如果品红褪色,加热后又恢复红色,证明有二氧化硫,
故答案为:将气体通入品红溶液中,如果品红褪色,加热后又恢复红色.
点评 本题考查了气体的实验室制法,要熟练掌握反应原理、发生装置的选择、收集装置的选择,题目难度不大.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
14.如图所示与对应叙述相符的是( )
| A. |  图甲表示一定温度下FeS和CuS的沉淀溶解平衡曲线,则Ksp(FeS)>Ksp(CuS) | |
| B. |  图乙表示pH=2的甲酸与乙酸溶液稀释时的pH变化曲线,则酸性:甲酸<乙酸 | |
| C. | 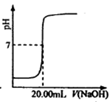 图丙表示用0.1000 mol•L-1NaOH溶液滴定25.00 mL盐酸的滴定曲线,则 c(HCl)=0.0800 mol•L-1 | |
| D. |  图丁表示反应N2(g)+3H2(g)?2NH3(g)平衡时NH3体积分数随起始<“m“:math dsi:zoomscale=150 dsi:_mathzoomed=1>n(N2)n(H2)$\frac{{n(N}_{2})}{n({H}_{2})}$变化的曲线,则转化率:αA(H2)=αB(H2) |
15.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 32克O2和O3组成的混合气体中含有的氧原子数目为2NA | |
| B. | 常温常压下,22.4 L乙醇含有的分子数目为NA | |
| C. | 1 mol Na变为Na+时得到的电子数目为NA | |
| D. | 1mol/L NaCl溶液中含有Na+个数为NA |
12.化学与社会、科学、技术、环境、生活等有密切关系,下列说法正确的是( )
| A. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| B. | 要除去衣服上的顽固污渍,均可将衣服泡在漂白液中 | |
| C. | 纤维素食用在人体内水解为葡萄糖为人体提供能量 | |
| D. | 葡萄中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒 |
19. 近年来AIST报告正在研制一种“高容量、低成本”锂一铜空气燃料电池.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )
近年来AIST报告正在研制一种“高容量、低成本”锂一铜空气燃料电池.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )
 近年来AIST报告正在研制一种“高容量、低成本”锂一铜空气燃料电池.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )
近年来AIST报告正在研制一种“高容量、低成本”锂一铜空气燃料电池.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )| A. | 放电时,Li+透过固体电解质向Cu极移动 | |
| B. | 整个反应过程中,铜相当于催化剂 | |
| C. | 通空气时,铜被氧化,表面产生Cu2O | |
| D. | Li电极减轻7g时,至少需消耗空气5.6L(标准状况) |
9. 硫化锌(ZnS)晶体用作分析试剂、荧光体、光导体材,久置湿空气中易被氧化为ZnSO4.回答下列问题:
硫化锌(ZnS)晶体用作分析试剂、荧光体、光导体材,久置湿空气中易被氧化为ZnSO4.回答下列问题:
(1)写出基态30Zn原子的价电子排布式3d104s2,基态S原子核外未成对电子数为2,有5种能量不同的电子.
(2)ZnSO4中三种元素的电负性由大到小的顺序为O>S>Zn,SO42-的立体构型为正四面体形,它的等电子体是$P{O}_{4}^{3-}$(任写一种),其中SO42-中S的杂化轨道类型为sp3.
(3)Zn(NH3)4]SO4晶体中不存在的微粒间作用力有D、E.
A.离子键 B.共价键 C.配位键 D.范德华力 E.氢键
(4)根据下列锌卤化物的熔点和溶解性,判断ZnF2晶体的类型为离子晶体;分析ZnCl2、ZnBr2、ZnI2熔点依次增大的原因ZnCl2、ZnBr2、ZnI2都是分子晶体,组成与结构相似,随着相对分子质量的增大,范德华力增强,熔沸点升高..
(5)立方ZnS晶体的密度为ρg•cm-3,其晶胞结构如图.Zn2+周围等距离且最近的Zn2+、S2-依次为12、4;ZnS晶胞中的晶胞参数a=$\root{3}{\frac{4×97}{ρ×{N}_{A}}}$cm(列出计算式).
 硫化锌(ZnS)晶体用作分析试剂、荧光体、光导体材,久置湿空气中易被氧化为ZnSO4.回答下列问题:
硫化锌(ZnS)晶体用作分析试剂、荧光体、光导体材,久置湿空气中易被氧化为ZnSO4.回答下列问题:(1)写出基态30Zn原子的价电子排布式3d104s2,基态S原子核外未成对电子数为2,有5种能量不同的电子.
(2)ZnSO4中三种元素的电负性由大到小的顺序为O>S>Zn,SO42-的立体构型为正四面体形,它的等电子体是$P{O}_{4}^{3-}$(任写一种),其中SO42-中S的杂化轨道类型为sp3.
(3)Zn(NH3)4]SO4晶体中不存在的微粒间作用力有D、E.
A.离子键 B.共价键 C.配位键 D.范德华力 E.氢键
(4)根据下列锌卤化物的熔点和溶解性,判断ZnF2晶体的类型为离子晶体;分析ZnCl2、ZnBr2、ZnI2熔点依次增大的原因ZnCl2、ZnBr2、ZnI2都是分子晶体,组成与结构相似,随着相对分子质量的增大,范德华力增强,熔沸点升高..
| ZnF2 | ZnCl2 | ZnBr2 | ZnI2 | |
| 熔点/℃ | 872 | 275 | 394 | 446 |
| 在乙醇、乙醚中溶解性 | 不溶 | 溶解 | 溶解 | 溶解 |
14.下列离子方程式书写正确的是( )
| A. | Cu(OH)2与稀硝酸反应:H++OH-=H2O | |
| B. | 铜片与浓硝酸反应:Cu+4H++2 NO3-=Cu2++2NO2↑+2H2O | |
| C. | 氨水与MgCl2溶液反应:Mg2++2OH-=Mg(OH)2↓ | |
| D. | 铁与稀硝酸反应:Fe+2H+=Fe2++H2↑ |


 .
.