题目内容
(2012?茂名二模)常温下,有物质的量浓度均为0.1mol?L-1的CH3COOH溶液和NaOH溶液,下列说法正确的是( )
分析:A、醋酸是弱电解质,存在电离平衡;
B、醋酸稀释氢离子浓度减小,氢氧根离子浓度增大;
C、量溶液等体积混合生成醋酸钠,醋酸根离子水解;
D、当溶液中含等浓度的醋酸和醋酸钠时存在c(CH3COO-)>c(Na+);
B、醋酸稀释氢离子浓度减小,氢氧根离子浓度增大;
C、量溶液等体积混合生成醋酸钠,醋酸根离子水解;
D、当溶液中含等浓度的醋酸和醋酸钠时存在c(CH3COO-)>c(Na+);
解答:解:A、0.1mol?L-1的CH3COOH溶液,醋酸是弱电解质存在电离平衡PH大于1,故A错误;
B、往醋酸溶液中加水,促进电离,c(H+)减小,依据离子积常数,c(OH-) 增大,故B错误;
C、两溶液等体积混合生成醋酸钠溶液,醋酸根水解,所以c(Na+)>c(CH3COO-),故C正确;
D、两溶液按一定体积比混合,反应后的溶液中若是等浓度的醋酸和醋酸钠,则存在:c(CH3COO-)>c(Na+),故D正确;
故选CD.
B、往醋酸溶液中加水,促进电离,c(H+)减小,依据离子积常数,c(OH-) 增大,故B错误;
C、两溶液等体积混合生成醋酸钠溶液,醋酸根水解,所以c(Na+)>c(CH3COO-),故C正确;
D、两溶液按一定体积比混合,反应后的溶液中若是等浓度的醋酸和醋酸钠,则存在:c(CH3COO-)>c(Na+),故D正确;
故选CD.
点评:本题考查了弱电解质的电离平衡,溶液稀释离子浓度的变化,离子浓度大小的分析判断,题目较难.

练习册系列答案
 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案
相关题目
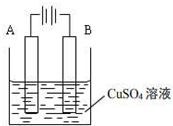 (2012?茂名二模)如图是某同学用Cu在Fe片上镀铜的实验装置,下列说法正确的是( )
(2012?茂名二模)如图是某同学用Cu在Fe片上镀铜的实验装置,下列说法正确的是( )