题目内容
下列有关电解质说法正确的是( )
| A、NH3、SO2的水溶液均导电,所以NH3、SO2均属于电解质 |
| B、强电解质饱和溶液一定比弱电解质饱和溶液的导电性强 |
| C、NaCl溶液能导电,故NaCl溶液为电解质 |
| D、NaHCO3是强电解质,故NaHCO3的电离方程式为NaHCO3═Na++HCO3- |
考点:电解质与非电解质
专题:电离平衡与溶液的pH专题
分析:A.电解质指:水溶液中或熔融状态下能够导电的化合物,注意能导电,必须是电解质自身电离出自由移动的离子;在上述两种情况下都不能导电的化合物称为非电解质;
B.溶液导电能力取决于溶液中离子浓度的大小,与电解质强弱无关;
C.根据电解质的概念分析解答;
D.碳酸氢钠为强电解质,溶液中电离出钠离子和碳酸氢根离子;
B.溶液导电能力取决于溶液中离子浓度的大小,与电解质强弱无关;
C.根据电解质的概念分析解答;
D.碳酸氢钠为强电解质,溶液中电离出钠离子和碳酸氢根离子;
解答:
解:A.氨气是化合物,溶于水,氨气和水反应生成一水和氨,NH3?H2O?NH4++OH-导电,但这些离子不是氨气电离,氨气是非电解质,SO2溶于水生成亚硫酸,亚硫酸电离出阴、阳离子而使其溶液导电,电离出阴阳离子的物质是亚硫酸,而不是SO2,所以SO2是非电解质,故A错误;
B.强弱电解质和电解质是否易溶于水无关,强电解质与电解质是否完全电离有关,硫酸钡难溶于水,但它是强电解质,乙酸易溶于水,但它是弱酸.强电解质溶液的导电性不一定比弱电解质溶液导电性强,故B错误;
C.电解质必须是化合物,NaCl溶液为混合物,故C错误;
D.碳酸氢钠属于强电解质,溶液中完全电离,碳酸氢钠的电离方程式为:NaHCO3═Na++HCO3-,故D正确;
故选D.
B.强弱电解质和电解质是否易溶于水无关,强电解质与电解质是否完全电离有关,硫酸钡难溶于水,但它是强电解质,乙酸易溶于水,但它是弱酸.强电解质溶液的导电性不一定比弱电解质溶液导电性强,故B错误;
C.电解质必须是化合物,NaCl溶液为混合物,故C错误;
D.碳酸氢钠属于强电解质,溶液中完全电离,碳酸氢钠的电离方程式为:NaHCO3═Na++HCO3-,故D正确;
故选D.
点评:本题考查侧重电解质和非电解质判断,根据概念来分析解答,明确碳酸氢钠为强电解质,溶液中电离出钠离子和碳酸氢根离子是解答该题的易错点,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
50mL 0.3mol/L的AlCl3溶液加水稀释到500mL,稀释后溶液中Cl-的物质的量浓度为( )
| A、0.03mol/L |
| B、0.09mol/L |
| C、0.045mol/L |
| D、0.015mol/L |
金属钠放在水中浮在水面上,放在煤油中沉在油层下,煤油的密度是0.8g?cm-3,推测钠的密度(g?cm-3)( )
| A、大于1.0g?cm-3 |
| B、小于0.8g?cm-3 |
| C、介于0.8~1.0g?cm-3之间 |
| D、不能确定 |
分类是化学研究中常用的方法.下列分类方法中正确的是( )
| A、根据元素原子最外层电子数的多少将元素分为金属和非金属 |
| B、依据组成元素的种类,将纯净物分为单质和化合物 |
| C、根据氧化物中是否含有金属元素,将氧化物分为碱性氧化物和酸性氧化物 |
| D、根据分散系的稳定性大小,将分散系分为胶体、浊液和溶液 |
CrO5的结构式为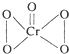 ,据此推断该氧化物( )
,据此推断该氧化物( )
 ,据此推断该氧化物( )
,据此推断该氧化物( )| A、稳定性比较高,不易分解 |
| B、稳定性比较低,易分解 |
| C、分子中所有原子均达到8电子稳定结构 |
| D、属于碱性氧化物 |
用密度为1.32g/cm3的硫酸溶液逐滴滴入到氢氧化钡溶液中,直到沉淀恰好完全为止.已知生成沉淀的质量等于原硫酸溶液的质量,硫酸溶液中溶质的质量分数是( )
| A、42.1% |
| B、43.1% |
| C、44.1% |
| D、45.1% |
不用其他试剂无法鉴别的一组溶液是( )
| A、氯化铁溶液和氯化铜溶液 |
| B、盐酸和碳酸氢钠溶液 |
| C、氯化铝溶液和氢氧化钠溶液 |
| D、硫酸溶液和碳酸钠溶液 |
常温下,四种溶液的pH如下:
下列说法正确的是( )
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠 | 醋酸 | 硫酸 |
| pH | 11 | 11 | 3 | 3 |
| A、在①、②中分别加入适量的(NH4)2SO4晶体后,①的pH减小,②的pH不变 |
| B、将V1 mL④溶液与 V2 mL②溶液混合后,测得混合溶液pH=4,则V1:V2=9:11 |
| C、分别加水稀释10倍,四种溶液的pH大小顺序为:①>②>③>④ |
| D、将①、④两种溶液等体积混合,所得溶液中:c(NH4+)>c(SO42-)>c(OH-)>c(H+) |