题目内容
碘钨灯具有使用寿命长、节能环保等优点.一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:W(s)+I2(g)  WI2(g)
WI2(g)
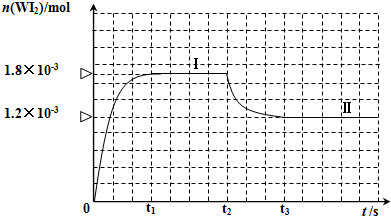
为模拟上述反应,在实验室中准确称取0.508g碘、0.736g金属钨放置于50.0mL密闭容器中,并加热使其反应.如图是混合气体中的WI2蒸气的物质的量随时间变化关系的图象[n(WI2)~t],其中曲线Ⅰ(0~t2时间段)的反应温度为450℃,曲线Ⅱ(从t2时刻开始)的反应温度为530℃.请回答下列问题:
(1)该反应的化学平衡常数表达式为:K=
(2)该反应是
(3)反应从开始到t1(t1=3min)时间内的平均速率:u(I2)=
(4)能够说明上述反应已经达到平衡状态的有
a.I2与WI2的浓度相等
b.单位时间内,金属钨消耗的物质的量与单质碘生成的物质的量相等
c.容器内混合气体的密度不再改变
d.容器内气体压强不发生变化
 WI2(g)
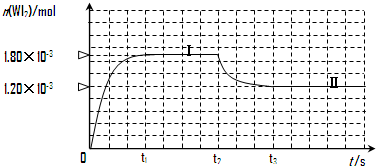
WI2(g)为模拟上述反应,在实验室中准确称取0.508g碘、0.736g金属钨放置于50.0mL密闭容器中,并加热使其反应.如图是混合气体中的WI2蒸气的物质的量随时间变化关系的图象[n(WI2)~t],其中曲线Ⅰ(0~t2时间段)的反应温度为450℃,曲线Ⅱ(从t2时刻开始)的反应温度为530℃.请回答下列问题:
(1)该反应的化学平衡常数表达式为:K=
| C(WI2) |
| C(I2) |
| C(WI2) |
| C(I2) |
(2)该反应是
放热
放热
(填“放热”或“吸热”)反应,判断依据是:温度升高,n(WI2)减小,平衡向左移动,所以是放热反应;
温度升高,n(WI2)减小,平衡向左移动,所以是放热反应;
.(3)反应从开始到t1(t1=3min)时间内的平均速率:u(I2)=
1.20×10-2mol?L-1?min-1
1.20×10-2mol?L-1?min-1
.(4)能够说明上述反应已经达到平衡状态的有
b、c
b、c
.a.I2与WI2的浓度相等
b.单位时间内,金属钨消耗的物质的量与单质碘生成的物质的量相等
c.容器内混合气体的密度不再改变
d.容器内气体压强不发生变化

分析:(1)据化学平衡常数的概念
(2)根据温度对化学平衡、化学平衡常数的影响;
(3)根据反应速率的公式进行计算;
(4)根据化学平衡的标志来判断;
(2)根据温度对化学平衡、化学平衡常数的影响;
(3)根据反应速率的公式进行计算;
(4)根据化学平衡的标志来判断;
解答:解:(1)因平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,所以K=
,故答案为:
;
(2)化学平衡常数的大小只与温度有关,升高温度,平衡向吸热的方向移动,由表可知:升高温度,WI2的物质的量减少,说明化学平衡逆向移动,因此正反应方向放热,故答案为:放热;温度升高,n(WI2)减小,平衡向左移动,所以是放热反应;
(3)从反应开始到t1时间内,结合图象,生成WI2(g)的物质的量为1.8×10-3mol,所以碘单质的物质的量减少1.8×10-3mol,根据公式v=
=
=
=1.20×10-2 mol?L-1?min-1,故答案为:1.20×10-2 mol?L-1?min-1;
(4)A、达到平衡状态时,各物质的浓度不变,不一定相等,故A错误;
B、单位时间内,金属钨消耗的物质的量与单质碘生成的物质的量相等,说明v逆=v正,故B正确;
C、由于反应物中有气体,只有在平衡状态,密度不变,故C正确;
D、因前后气体分子数相等,则无论是否达到平衡状态,压强不变,故D错误;
故选:b、c.
| C(WI2) |
| C(I2) |
| C(WI2) |
| C(I2) |
(2)化学平衡常数的大小只与温度有关,升高温度,平衡向吸热的方向移动,由表可知:升高温度,WI2的物质的量减少,说明化学平衡逆向移动,因此正反应方向放热,故答案为:放热;温度升高,n(WI2)减小,平衡向左移动,所以是放热反应;
(3)从反应开始到t1时间内,结合图象,生成WI2(g)的物质的量为1.8×10-3mol,所以碘单质的物质的量减少1.8×10-3mol,根据公式v=
| △c |
| △t |
| ||
| △t |
| ||
| 3min |
(4)A、达到平衡状态时,各物质的浓度不变,不一定相等,故A错误;
B、单位时间内,金属钨消耗的物质的量与单质碘生成的物质的量相等,说明v逆=v正,故B正确;
C、由于反应物中有气体,只有在平衡状态,密度不变,故C正确;
D、因前后气体分子数相等,则无论是否达到平衡状态,压强不变,故D错误;
故选:b、c.
点评:本题主要考查温度对化学平衡、化学平衡常数的影响以及平衡的判断,难度不大,考查学生分析和解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
(12分)(每空3分)碘钨灯具有使用寿命长、节能环保等优点。一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:
W(s)+ I2(g) WI2(g)ΔH<0
WI2(g)ΔH<0
为模拟上述反应,在450℃时向一体积为2L的恒容密闭容器中加入0.1mol碘单质和足量的钨,2min后反应达到平衡,测得碘蒸气浓度为0.005 mol·L-1。请回答下列问题:
(1)前两分钟内碘蒸气的反应速率为 。
(2)能够说明上述反应已经达到平衡状态的有 。
| A.I2与WI2的浓度相等 |
| B.容器内气体压强不再变化 |
| C.W的质量不再变化 |
| D.单位时间内,金属钨消耗的物质的量与碘化钨生成的物质的量相等 |
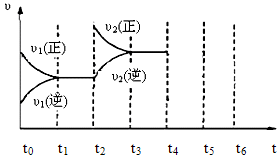
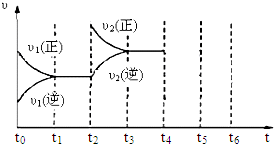
(3)下图为该反应在450℃时的时间—速率图,则t2时刻改变的外界条件可能是 ,若t4时刻将容器压缩至一半(各物质状态不变),保持该条件至t6,请在图中画出t4到t6时间段内大致曲线图,并在相应曲线上标上υ3(正)、υ3(逆)
 WI2(g)
WI2(g)