题目内容
已知:Pb的化合价只有+2、+4,且+4价的Pb具有强氧化性,能氧化浓盐酸生成C12;
(1)写出Pb3O4与浓盐酸反应的化学方程式______.
(2)PbO2不稳定,随温度升高按下列顺序逐步分解:PbO2→Pb2O3→Pb3O4→PbO.若加热分解后所得到的固体全部为Pb3O4,现将a mol PbO2加热分解,则加热过程中放出O2______L(标准状况下);
(3)现将1mol PbO2加热分解,收集产生的O2,加热分解后所得固体中,pb2+占Pb元素的物质的量分数为x;再向加热所得固体中加入足量的浓盐酸,收集产生的C12,收集到O2和C12的物质的量之和为y mol.
试回答下列问题:
①确定y与x的函数关系式为______.
②若两步反应中O2和Cl2的物质的量之比为3:5,则剩余固体中含有的物质为______,其物质的量之比为______.
解:(1)Pb3O4中Pb的化合价只有+2、+4,再根据化合价代数和等于零,求得Pb的总化合价为+8价,即可确定Pb3O4中有一个+4价、有两个+2价,且+4价的Pb具有强氧化性,能氧化浓盐酸生成C12,本身被还原成+2价Pb,生成PbC12,
根据元素守恒得反应物与生成物:Pb3O4+HCl(浓)→PbCl2+Cl2↑+H2O,根据化合价升降法配平该氧化还原反应,
Pb3O4中一个+4价的Pb降低到+2价,降低2价;HCl(浓)中-1价的Cl上升到0价生成Cl2,上升1价×2,所以Pb3O4和Cl2前面的计量数都为1,根据原子守恒配平其它物质前计量数,得各物质前计量数为1、8、3、1、4,故方程式为Pb3O4+8HCl(浓)═3PbCl2+Cl2↑+4H2O,
故答案为:Pb3O4+8HCl(浓)═3PbCl2+Cl2↑+4H2O;
(2)根据题意,确定反应物为PbO2,生成物为Pb3O4和O2,因此方程式为 3PbO2 Pb3O4+O2,
Pb3O4+O2,
设生成氧气物质的量为x,
3PbO2 Pb3O4+O2
Pb3O4+O2
3mol 1mol
amol x
解得:x═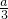 mol
mol
则V(O2)═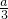 mol×22.4L/mol═
mol×22.4L/mol═ L,
L,
故答案为: L;
L;
(3)①根据题意:1mol PbO2分解所得混合物中n(Pb2+)=x mol、n(Pb4+)=(1-x) mol.在反应过程中1mol PbO2中+4价的Pb具有强氧化性作氧化剂,
+4价的Pb最终全部降低为+2价,
根据得失电子守恒:先加热分解生成O2,得n(O2)═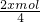 ═
═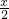 mol;
mol;
后再与足量的浓盐酸反应生成Cl2,得n(Cl2)═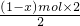 ═(1-x) mol,
═(1-x) mol,
则 y═n(O2)+n(Cl2)═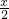 mol+(1-x) mol═(1-
mol+(1-x) mol═(1-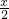 )mol,
)mol,
故答案为:y═(1-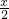 )mol;
)mol;
②若两步反应中O2和Cl2的物质的量之比为3:5,
根据上述分析:n(O2)═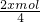 ═
═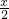 mol,n(Cl2)═
mol,n(Cl2)═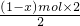 ═(1-x) mol
═(1-x) mol
即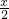 :(1-x)═3:5,
:(1-x)═3:5,
解得:x═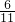 ,
,
则剩余固体中含pb2+的物质的量分数为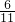 ,含pb4+的物质的量分数为
,含pb4+的物质的量分数为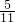 ,即n(pb2+):n(pb4+)═6:5,
,即n(pb2+):n(pb4+)═6:5,
由题意,PbO2不稳定逐步分解顺序:PbO2→Pb2O3→Pb3O4→PbO.因为Pb的化合价只有+2、+4,所以Pb2O3可表示为
PbO?PbO2,Pb3O4可表示为2PbO?PbO2,各氧化物中n(pb2+):n(pb4+)的比值关系为:
PbO2中,n(pb2+):n(pb4+)═0:1
Pb2O3中,n(pb2+):n(pb4+)═1:1
Pb3O4中,n(pb2+):n(pb4+)═2:1
PbO中,n(pb2+):n(pb4+)═1:0
根据剩余固体中n(pb2+):n(pb4+)═6:5,介于1:1和2:1之间,可推出剩余固体中所含物质为Pb2O3、Pb3O4.
设剩余固体中Pb2O3物质的量为a、Pb3O4物质的量为b,
得n(pb2+)═a+2b,n(pb4+)═a+b,
则(a+2b):(a+b)═6:5
解得a:b═4:1,即(Pb2O3):(Pb3O4)═4:1,
故答案为:Pb2O3、Pb3O4;4:1.
分析:(1)Pb3O4中+4价的Pb具有强氧化性,能氧化浓盐酸,+4价的Pb被浓盐酸还原成+2价,确定生成物PbC12、C12、H2O,再配平可得化学方程式;
(2)根据题意,确定反应物为PbO2,生成物为Pb3O4和O2,写出方程式,再利用方程式进行计算求解;
(3)根据氧化还原反应的本质电子得失守恒求出n(O2)、n(Cl2),即得y与x的函数关系.根据两步反应中O2和Cl2的物质的量之比为3:5,求出x的值,确定出
n(pb2+):n(pb4+)的比值,再设法求解.
点评:本题考查氧化还原反应知识,利用化合价升降法配平,抓住本质电子的得失守恒是解题的关键,同时结合中间值确定反应产物.该题对抽象思维能力要求较高,很容易感觉无从下笔,难度较大.
根据元素守恒得反应物与生成物:Pb3O4+HCl(浓)→PbCl2+Cl2↑+H2O,根据化合价升降法配平该氧化还原反应,
Pb3O4中一个+4价的Pb降低到+2价,降低2价;HCl(浓)中-1价的Cl上升到0价生成Cl2,上升1价×2,所以Pb3O4和Cl2前面的计量数都为1,根据原子守恒配平其它物质前计量数,得各物质前计量数为1、8、3、1、4,故方程式为Pb3O4+8HCl(浓)═3PbCl2+Cl2↑+4H2O,
故答案为:Pb3O4+8HCl(浓)═3PbCl2+Cl2↑+4H2O;
(2)根据题意,确定反应物为PbO2,生成物为Pb3O4和O2,因此方程式为 3PbO2
 Pb3O4+O2,
Pb3O4+O2,设生成氧气物质的量为x,
3PbO2
 Pb3O4+O2
Pb3O4+O23mol 1mol
amol x
解得:x═
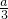 mol
mol则V(O2)═
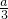 mol×22.4L/mol═
mol×22.4L/mol═ L,
L,故答案为:
 L;
L;(3)①根据题意:1mol PbO2分解所得混合物中n(Pb2+)=x mol、n(Pb4+)=(1-x) mol.在反应过程中1mol PbO2中+4价的Pb具有强氧化性作氧化剂,
+4价的Pb最终全部降低为+2价,
根据得失电子守恒:先加热分解生成O2,得n(O2)═
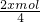 ═
═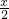 mol;
mol;后再与足量的浓盐酸反应生成Cl2,得n(Cl2)═
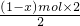 ═(1-x) mol,
═(1-x) mol,则 y═n(O2)+n(Cl2)═
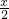 mol+(1-x) mol═(1-
mol+(1-x) mol═(1-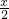 )mol,
)mol,故答案为:y═(1-
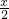 )mol;
)mol;②若两步反应中O2和Cl2的物质的量之比为3:5,
根据上述分析:n(O2)═
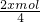 ═
═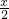 mol,n(Cl2)═
mol,n(Cl2)═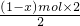 ═(1-x) mol
═(1-x) mol即
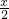 :(1-x)═3:5,
:(1-x)═3:5,解得:x═
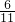 ,
,则剩余固体中含pb2+的物质的量分数为
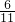 ,含pb4+的物质的量分数为
,含pb4+的物质的量分数为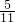 ,即n(pb2+):n(pb4+)═6:5,
,即n(pb2+):n(pb4+)═6:5,由题意,PbO2不稳定逐步分解顺序:PbO2→Pb2O3→Pb3O4→PbO.因为Pb的化合价只有+2、+4,所以Pb2O3可表示为
PbO?PbO2,Pb3O4可表示为2PbO?PbO2,各氧化物中n(pb2+):n(pb4+)的比值关系为:
PbO2中,n(pb2+):n(pb4+)═0:1
Pb2O3中,n(pb2+):n(pb4+)═1:1
Pb3O4中,n(pb2+):n(pb4+)═2:1
PbO中,n(pb2+):n(pb4+)═1:0
根据剩余固体中n(pb2+):n(pb4+)═6:5,介于1:1和2:1之间,可推出剩余固体中所含物质为Pb2O3、Pb3O4.
设剩余固体中Pb2O3物质的量为a、Pb3O4物质的量为b,
得n(pb2+)═a+2b,n(pb4+)═a+b,
则(a+2b):(a+b)═6:5
解得a:b═4:1,即(Pb2O3):(Pb3O4)═4:1,
故答案为:Pb2O3、Pb3O4;4:1.
分析:(1)Pb3O4中+4价的Pb具有强氧化性,能氧化浓盐酸,+4价的Pb被浓盐酸还原成+2价,确定生成物PbC12、C12、H2O,再配平可得化学方程式;
(2)根据题意,确定反应物为PbO2,生成物为Pb3O4和O2,写出方程式,再利用方程式进行计算求解;
(3)根据氧化还原反应的本质电子得失守恒求出n(O2)、n(Cl2),即得y与x的函数关系.根据两步反应中O2和Cl2的物质的量之比为3:5,求出x的值,确定出
n(pb2+):n(pb4+)的比值,再设法求解.
点评:本题考查氧化还原反应知识,利用化合价升降法配平,抓住本质电子的得失守恒是解题的关键,同时结合中间值确定反应产物.该题对抽象思维能力要求较高,很容易感觉无从下笔,难度较大.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目