题目内容
(2011?新疆二模)把一块镁铝合金投入到1mol/L HCl溶液里,待合金完全溶解后,往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积(单位mL)变化的关系如下图A所示.下列说法中不正确的是( )

分析:A、根据第三阶段的反应确定铝离子的物质的量,假设只有铝离子时,根据消耗的氢氧化钠来确定a的取值范围;
B、根据第三阶段的反应确定铝离子的物质的量,所以铝离子生成氢氧化铝所需的氢氧化钠的物质的量一定,根据a的取值判断镁的物质的量;
C、采用极值法计算,当没有铝离子时,a值最小,当生成的沉淀全部是氢氧化铝时,a值最大.
D、采用极值法计算,当没有铝离子时,a值最大,当生成的沉淀全部是氢氧化铝时,a值最小.
B、根据第三阶段的反应确定铝离子的物质的量,所以铝离子生成氢氧化铝所需的氢氧化钠的物质的量一定,根据a的取值判断镁的物质的量;
C、采用极值法计算,当没有铝离子时,a值最小,当生成的沉淀全部是氢氧化铝时,a值最大.
D、采用极值法计算,当没有铝离子时,a值最大,当生成的沉淀全部是氢氧化铝时,a值最小.
解答:解:A、第三阶段,氢氧化铝溶解Al(OH)3 +NaOH=NaAlO2+2H2O,因为此时消耗NaOH10mL,所以n(Al3+)=0.01mol,和Al3+反应的NaOH为30mL,因为第一阶段和Al3+反应的NaOH为30mL,假设无Mg2+,a=50,而实际存在Mg2+,当没有盐酸剩余时,a=0,所以0≤a<50,故A正确.
B、第三阶段,氢氧化铝溶解Al(OH)3 +NaOH=NaAlO2+2H2O,因为此时消耗NaOH10mL,所以n(Al3+)=n(Al)=0.01mol,和Al3+反应的NaOH为30mL,因为第一阶段和Al3+反应的NaOH为30mL;当a=0时,盐酸没有剩余,与氢氧化钠反应的离子是镁离子和铝离子,铝离子一定,镁离子物质的量最大,与镁离子反应的氢氧化钠的体积为50mL,50mL氢氧化钠的物质的量为0.05mol,镁离子的物质的量是0.025mol,所以
=
=2.5,故B正确.
C、采用极值法计算,当没有铝离子时,生成的沉淀不和氢氧化钠反应导致a值最小,80=a;当生成的沉淀全部是氢氧化铝时,氢氧化铝能和氢氧化钠反应生成偏铝酸钠,导致a值最大,生成氢氧化铝沉淀所用的氢氧化钠体积是溶解氢氧化铝所用氢氧化钠体积的3倍,所以溶解氢氧化铝所用氢氧化钠的体积为
,a=96.7,实际上存在镁离子,所以a的取值范围是80<a<96.7,故C错误.
D、采用极值法计算,当没有铝离子时,生成的沉淀全部是氢氧化镁,氢氧化镁和氢氧化钠不反应,此时a值最大为90;当生成的沉淀全部是氢氧化铝,生成的氢氧化铝又能和氢氧化钠完全转化为偏铝酸钠时a值最小,生成氢氧化铝所用的氢氧化钠与溶解氢氧化铝所用的氢氧化钠的体积之比=3:1,所以a=
×3+30=75,实际上溶液中含有铝离子和镁离子,所以a的取值范围是75<a<90,故D正确.
故选C.
B、第三阶段,氢氧化铝溶解Al(OH)3 +NaOH=NaAlO2+2H2O,因为此时消耗NaOH10mL,所以n(Al3+)=n(Al)=0.01mol,和Al3+反应的NaOH为30mL,因为第一阶段和Al3+反应的NaOH为30mL;当a=0时,盐酸没有剩余,与氢氧化钠反应的离子是镁离子和铝离子,铝离子一定,镁离子物质的量最大,与镁离子反应的氢氧化钠的体积为50mL,50mL氢氧化钠的物质的量为0.05mol,镁离子的物质的量是0.025mol,所以
| n(Mg) |
| n(Al) |
| 0.025mol |
| 0.01mol |
C、采用极值法计算,当没有铝离子时,生成的沉淀不和氢氧化钠反应导致a值最小,80=a;当生成的沉淀全部是氢氧化铝时,氢氧化铝能和氢氧化钠反应生成偏铝酸钠,导致a值最大,生成氢氧化铝沉淀所用的氢氧化钠体积是溶解氢氧化铝所用氢氧化钠体积的3倍,所以溶解氢氧化铝所用氢氧化钠的体积为
| 50 |
| 3 |
D、采用极值法计算,当没有铝离子时,生成的沉淀全部是氢氧化镁,氢氧化镁和氢氧化钠不反应,此时a值最大为90;当生成的沉淀全部是氢氧化铝,生成的氢氧化铝又能和氢氧化钠完全转化为偏铝酸钠时a值最小,生成氢氧化铝所用的氢氧化钠与溶解氢氧化铝所用的氢氧化钠的体积之比=3:1,所以a=
| 90-30 |
| 4 |
故选C.
点评:本题考查学生有关金属元素铝及其化合物的性质的知识,结合图象进行考查,增大了难度,明确生成氢氧化铝所用的氢氧化钠与溶解氢氧化铝所用的氢氧化钠的体积之比=3:1是解本题的关键.

练习册系列答案
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
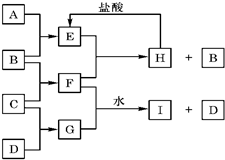 金属元素与金属元素的原子个数比为1:2.在一定条件下,各物质之间的相互转化关系如图(图中部分产物未列出):请填写下列空白:
金属元素与金属元素的原子个数比为1:2.在一定条件下,各物质之间的相互转化关系如图(图中部分产物未列出):请填写下列空白: