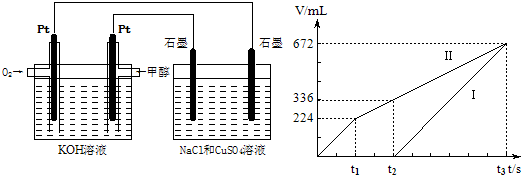
��Ŀ����
��16�֣��״���һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ������ҵ��һ��ɲ������·�Ӧ���ϳɼ״��� CO(g)+2H2(g)
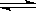 CH3OH(g) ��H<
0��
CH3OH(g) ��H<
0��
��1��������Ӧ��ƽ�ⳣ������ʽΪK= �������й�˵����ȷ����________
a�����¡����������£������ڵ�ѹǿ�������仯����淴Ӧ�ﵽƽ��
b��һ�������£�H2������������CO���������ʵ�2��ʱ���淴Ӧ�ﵽƽ��
c����������������䣬�����¶ȿ����CO��ת����
d��ʹ�ú��ʵĴ��������̴ﵽƽ���ʱ�䲢���CH3OH�IJ���
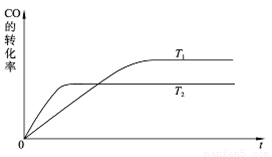
��2������������ͬʱ����T1��T2��T1< T2��������ͬ�¶��¿��淴Ӧ�ﵽƽ�⣬�뻭��CO��ת������ʱ��仯��ʾ��ͼ��

��3����֪�ڳ��³�ѹ�£�
�� 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ��H �� -a kJ��mol-1
�� 2CO(g)+O2(g)=2CO2(g) ��H �� -b kJ��mol-1
�� H2O(g)= H2O(l) ��H�� -c kJ��mol-1
�� CH3OH(l)+ O2(g) = CO (g) + 2H2O(l) ��H��______________kJ��mol-1��
��4��2009��10�£��й���ѧԺ����Ӧ�û�ѧ�о����ڼ״�ȼ�ϵ�ؼ�����������ͻ�ƣ���װ�����Ժ�����ؼ�����ʽ��ѡ��״�ȼ�ϵ�صĹ���ԭ����ͼ��ʾ��
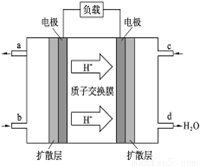
C�������ĵ缫��ӦʽΪ:___________________________������һ��ʱ���6.4 g�״���ȫ��Ӧ����CO2ʱ����______NA�����ӷ���ת�ơ�
��H��1 C��12 O��16��
��16�֣�
��1��c(CH3OH) / c(CO)c2(H2) (2��) ��A��3�֣�
��2����4�֣�
��3����b-a-4c��/ 2��2�֣�
��4��O2+4e-+4H+ = 2H2O��3�֣���1.2��2�֣�
����������1��a���ÿ��淴Ӧ������Ӧ����ϵ����ͬ����������ѹǿ�Ǹ���������ʱ�㶨�ˣ���˵���ﵽƽ�⡣
b��ֻ��������������Ӧ���ʣ�������˵�����淴Ӧ������ȣ�����
c�� ����Ӧ�Ƿ��ȷ�Ӧ������ƽ�������ƶ���CO��ת���ʽ���
d�������ɸı䷴Ӧ���ʵ����ܸı�ƽ��״̬�����ʵ�ת����
��2���ÿ��淴Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����£���Ӧ���ʼӿ죬�ﵽƽ������ʱ��̣�ƽ�������ƶ���CO��ת���ʽ���
��3���ɸ�˹���ɿɵ��ܷ�Ӧ�����٣���+4���ۣ�/2
��4���������������ƶ��������ڷ�Ӧ�еõ����ӣ����������ͨ��������������Ե缫��ӦʽΪO2��4e����4H��=2H2O��
����ܷ�ӦΪ��2CH3OH��3O2=2CO2��4H2O����Ӧ�е���ת��Ϊ12e�����ʵ�6.4 g�״���ȫ��Ӧʱ��1.2NA�����ӷ���ת��

 ����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
����ѧ�䵥Ԫ������ĩר����100��ϵ�д� �Ƹ�360�ȶ����ܾ�ϵ�д�
�Ƹ�360�ȶ����ܾ�ϵ�д� ���⿼����Ԫ���Ծ�ϵ�д�
���⿼����Ԫ���Ծ�ϵ�д� ��У���˳�̾�ϵ�д�
��У���˳�̾�ϵ�д�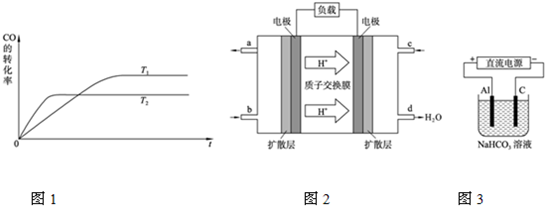
 ��Դ��ȱ���������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��Դ��ȱ���������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����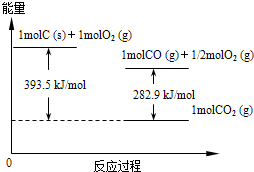 ��2012?������һģ����Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��2012?������һģ����Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����