题目内容
【题目】下列各图像中,不正确的是( )
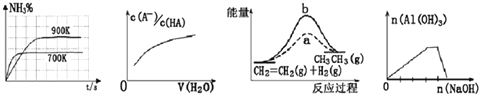
A. N2(g)+3H2(g)2NH3(g) △H=-92.4kJ/mol
B. 向弱酸HA的稀溶液中加水稀释
C. 有正催化剂(a)和无催化剂(b)时反应的能量变化
D. 向NH4Al(SO4)2溶液中滴加过量的NaOH溶液
【答案】A
【解析】A、温度升高,反应速率增大,到达平衡用的时间少,反应曲线的斜率大,并且该反应为放热反应,升高温度平衡向逆反应方向移动,氨气的含量降低,故A错误;B、向弱酸HA的稀溶液中加水稀释,促进弱酸的电离,平衡向正反应方向移动,则n(A-)增加,n(HA)减少,根据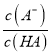 =
=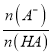 可知加水稀释时
可知加水稀释时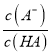 增大,故B正确;C、催化剂降低反应的活化能,但不能改变反应热,因此反应物和生成物的能量不变,故C正确;D、向NH4Al(SO4)2溶液中滴加过量NaOH溶液,首先发生反应为Al3++3OH-═Al(OH)3,当沉淀完全时,NH4+与OH-离子发生反应:NH4++OH-═NH3H2O,此时沉淀的质量不变,继续加NaOH,之后Al(OH)3继续与OH-离子反应:Al(OH)3+OH-═AlO2-+2H2O,故D正确;故选A。
增大,故B正确;C、催化剂降低反应的活化能,但不能改变反应热,因此反应物和生成物的能量不变,故C正确;D、向NH4Al(SO4)2溶液中滴加过量NaOH溶液,首先发生反应为Al3++3OH-═Al(OH)3,当沉淀完全时,NH4+与OH-离子发生反应:NH4++OH-═NH3H2O,此时沉淀的质量不变,继续加NaOH,之后Al(OH)3继续与OH-离子反应:Al(OH)3+OH-═AlO2-+2H2O,故D正确;故选A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目