题目内容
已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;镁和钠的化学性质也有一定的相似性。
两个研究性学习小组分别根据不同的微型课题进行研究,其方案如下:

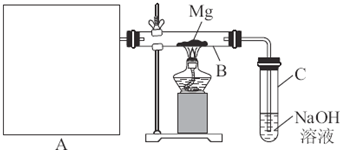
Ⅰ.第一个研究性学习小组用如图所示的装置进行镁与二氧化硫反应的实验。
(1)实验室制取二氧化硫类似于制取二氧化碳,在下列物质中选择合适的试剂制取二氧化硫:______________________。
A.10%的硫酸 B.80%的硫酸
C.浓盐酸 D.稀硝酸
E.亚硫酸钠固体 F.亚硫酸钙固体
G.饱和亚硫酸钠溶液
(2)反应后,发现B管壁有淡黄色固体粉末产生,取反应后B中固体溶于稀盐酸中产生具有臭鸡蛋气味的气体,写出B管中发生的有关化学反应方程式:______________________。
(3)你认为该装置是否有不足之处?______________。如果有,请写出改进方法:______________________________。
Ⅱ.第二个研究性学习小组进行了“实验室制硅”的研究,它们以课本为基础,查阅资料得到以下可供参考的信息:①工业上在高温时用木炭粉还原二氧化硅可制得硅 ②镁在点燃条件下即可与二氧化硅反应 ③金属硅化物与稀硫酸反应生成硫酸盐与硅烷 ④硅和二氧化硅均不与稀硫酸反应 ⑤硅烷在空气中能自燃
他们在研究报告中记载着“……选用合适的物质在适宜的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥,最后称量……在用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右”。
(4)该小组“实验室制硅”的化学方程式是_________________________________________。
(5)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是_________________。
(1)B、E
(2)2Mg+SO2![]() 2MgO+S,S+Mg
2MgO+S,S+Mg![]() MgS
MgS
(3)有 ①C试管的塞子换成双孔塞,另一孔插入一根直导管;②在A、B之间加一个干燥管
(4)2Mg+SiO2![]() 2MgO+Si
2MgO+Si
(5)金属镁与生成的硅继续反应生成硅化镁,硅化镁与稀H2SO4反应生成的SiH4可自燃(或用反应式说明:2Mg+SiO2![]() 2MgO+Si,2Mg+Si
2MgO+Si,2Mg+Si![]() Mg2Si,Mg2Si+2H2SO4====2MgSO4
Mg2Si,Mg2Si+2H2SO4====2MgSO4
+SiH4↑,SiH4+2O2====SiO2+2H2O)
解析:
Ⅰ.实验室利用亚硫酸盐与强酸反应制SO2,不同于CO2的是SO2具有强还原性,且溶于水,所以应选择固体亚硫酸盐与难挥发性强酸反应制取SO2,酸的浓度较大好些。亚硫酸钙与硫酸反应会生成硫酸钙微溶物附着在固体表面阻碍了固体与酸进一步反应。综上所述,应选择较浓的H2SO4与Na2SO3固体反应制取SO2。分析装置知,产生的SO2没有干燥,水蒸气会与镁反应;C试管只能进气,不能出气,不能维持气压平衡。二氧化硫与镁反应类似于二氧化碳与镁反应,产生的硫继续与镁反应生成硫化镁。
Ⅱ.强调“实验室制法”而不是“工业制法”。根据研究报告知,固体成分主要是硅化镁,与硫酸反应产生能在空气中自燃的硅烷。由此推知,用二氧化硅与镁反应先生成氧化镁和硅,硅与镁反应生成硅化镁。