题目内容
(2011?崇明县一模)在元素周期表中,相邻近的元素在结构和性质上有相似之处.
(1)例如:第二周期的Be与第三周期Al.
①Al原子的最外层电子排布式为
②Be 的氧化物的化学式为
(2)物质的化学键键能是指气态原子间形成1mol化学键释放的能量,如H(g)+I(g)→H-I(g)+297kJ H-I的键能为297kJ/mol,也可以理解为破开1mol H-I 键需要吸收297kJ的热量.下表是一些键能数据
根据表中数据回答下列问题:
①判断CCl4的稳定性
②卤代烃在同样条件下发生碱性水解时,RF、RCl、RBr、RI(R为相同的烃基)反应活性由大到小的顺序的是
③下列关于水和硫化氢的讨论正确的是
(1)例如:第二周期的Be与第三周期Al.
①Al原子的最外层电子排布式为
3s23p1
3s23p1
,其最高价氧化物对应的水化物在碱性溶液中的电离方程式为Al(OH)3?AlO2-+H++H2O
Al(OH)3?AlO2-+H++H2O
.②Be 的氧化物的化学式为
BeO
BeO
,其最高价氧化物对应的水化物分别与足量NaOH溶液和盐酸反应的化学方程式为Be(OH)2+2NaOH=Na2BeO2+H2O
Be(OH)2+2NaOH=Na2BeO2+H2O
、Be(OH)2+2HCl=BeCl2+H2O
Be(OH)2+2HCl=BeCl2+H2O
.(2)物质的化学键键能是指气态原子间形成1mol化学键释放的能量,如H(g)+I(g)→H-I(g)+297kJ H-I的键能为297kJ/mol,也可以理解为破开1mol H-I 键需要吸收297kJ的热量.下表是一些键能数据
| 键能(kJ/mol) | 键能(kJ/mol) | 键能(kJ/mol) | |||
| H-H | 436 | C-Cl | 243 | H-Cl | 432 |
| Cl-Cl | 330 | C-I | 218 | C-F | 427 |
| C-O | 347 | H-O | 464 | H-F | 565 |
①判断CCl4的稳定性
小于
小于
(填“大于”或“小于”)CF4 的稳定性.②卤代烃在同样条件下发生碱性水解时,RF、RCl、RBr、RI(R为相同的烃基)反应活性由大到小的顺序的是
RI>RBr>RCl>RF
RI>RBr>RCl>RF
.③下列关于水和硫化氢的讨论正确的是
C
C
(填编号)| 选项 | 现象:沸点H2O>H2S | 原理:键能H-O>H-S | 原理对现象的解释 |
| A | 正确 | 正确 | 可以 |
| B | 错误 | 正确 | |
| C | 正确 | 错误 | |
| D | 正确 | 正确 | 不可以 |
分析:(1)①根据核外电子排布规律书写Al的外围电子排布;
氢氧化铝在碱性溶液中发生酸式电离,电离出偏铝酸根、氢离子,同时生成水;
②Be处于第ⅡA族,氧化物中Be为+2价,据此书写氧化物化学式;
Be(OH)2的性质与氢氧化铝类似,故与氢氧化钠反应生成Na2BeO2、H2O,与盐酸反应生成BeCl2、H2O;
(2)①键能越大化学键越稳定,物质的稳定性越强;
②键能越小化学键越不稳定,卤代烃在同样条件下发生碱性水解越容易进行,反应活性越大;
③由于水分子之间存在氢键,常温下水为液体,硫化氢为气体,水的沸点更高,与键能无关,同主族自上而下原子半径增大,故键能H-O>H-S.
氢氧化铝在碱性溶液中发生酸式电离,电离出偏铝酸根、氢离子,同时生成水;
②Be处于第ⅡA族,氧化物中Be为+2价,据此书写氧化物化学式;
Be(OH)2的性质与氢氧化铝类似,故与氢氧化钠反应生成Na2BeO2、H2O,与盐酸反应生成BeCl2、H2O;
(2)①键能越大化学键越稳定,物质的稳定性越强;
②键能越小化学键越不稳定,卤代烃在同样条件下发生碱性水解越容易进行,反应活性越大;
③由于水分子之间存在氢键,常温下水为液体,硫化氢为气体,水的沸点更高,与键能无关,同主族自上而下原子半径增大,故键能H-O>H-S.
解答:解:(1)①Al原子有3个电子层,最外层电子数为3,Al的外围电子排布为3s23p1;
氢氧化铝在碱性溶液中发生酸式电离,电离出偏铝酸根、氢离子,同时生成水,电离方程式为Al(OH)3?AlO2-+H++H2O,
故答案为:3s23p1;Al(OH)3?AlO2-+H++H2O;
②Be处于第ⅡA族,氧化物中Be为+2价,氧化物化学式为BeO,Be(OH)2的性质与氢氧化铝类似,故与氢氧化钠反应生成Na2BeO2、H2O,方程式为Be(OH)2+2NaOH=Na2BeO2+H2O,与盐酸反应生成BeCl2、H2O,方程式为:Be(OH)2+2HCl=BeCl2+H2O,
故答案为:BeO;Be(OH)2+2NaOH=Na2BeO2+H2O;Be(OH)2+2HCl=BeCl2+H2O;
(2)①键能越大化学键越稳定,物质的稳定性越强,由表中数据可知,键能C-Cl<C-F,故CCl4的稳定性小于CF4 的稳定性,故答案为:小于;
②同主族自上而下,卤原子半径增大,故C-X(X代表卤原子)键能减小,键能越小化学键越不稳定,卤代烃在同样条件下发生碱性水解越容易进行,反应活性越大,故反应活性RI>RBr>RCl>RF,故答案为:RI>RBr>RCl>RF;
③由于水分子之间存在氢键,常温下水为液体,硫化氢为气体,水的沸点更高,与键能无关,同主族自上而下原子半径增大,故键能H-O>H-S,故选D.
氢氧化铝在碱性溶液中发生酸式电离,电离出偏铝酸根、氢离子,同时生成水,电离方程式为Al(OH)3?AlO2-+H++H2O,
故答案为:3s23p1;Al(OH)3?AlO2-+H++H2O;
②Be处于第ⅡA族,氧化物中Be为+2价,氧化物化学式为BeO,Be(OH)2的性质与氢氧化铝类似,故与氢氧化钠反应生成Na2BeO2、H2O,方程式为Be(OH)2+2NaOH=Na2BeO2+H2O,与盐酸反应生成BeCl2、H2O,方程式为:Be(OH)2+2HCl=BeCl2+H2O,
故答案为:BeO;Be(OH)2+2NaOH=Na2BeO2+H2O;Be(OH)2+2HCl=BeCl2+H2O;
(2)①键能越大化学键越稳定,物质的稳定性越强,由表中数据可知,键能C-Cl<C-F,故CCl4的稳定性小于CF4 的稳定性,故答案为:小于;
②同主族自上而下,卤原子半径增大,故C-X(X代表卤原子)键能减小,键能越小化学键越不稳定,卤代烃在同样条件下发生碱性水解越容易进行,反应活性越大,故反应活性RI>RBr>RCl>RF,故答案为:RI>RBr>RCl>RF;
③由于水分子之间存在氢键,常温下水为液体,硫化氢为气体,水的沸点更高,与键能无关,同主族自上而下原子半径增大,故键能H-O>H-S,故选D.
点评:本题考查元素周期表后元素周期律的综合应用,难度中等,注意基础知识的理解掌握.

练习册系列答案
相关题目
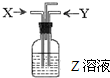 (2011?崇明县一模)如图,下列各组中,一定量的气体X和一定量的气体Y同时通入盛有溶液Z的洗气瓶中,最终肯定有沉淀生成的是(假定实验过程中不发生倒吸现象)…( )
(2011?崇明县一模)如图,下列各组中,一定量的气体X和一定量的气体Y同时通入盛有溶液Z的洗气瓶中,最终肯定有沉淀生成的是(假定实验过程中不发生倒吸现象)…( )