题目内容
在同温同压下,11.5g气体A所占的体积和8gO2 所占的体积相同,则气体A的相对分子质量为
- A.46
- B.28
- C.44
- D.64
A
分析:根据n= 计算氧气的物质的量,同温同压下,二者体积相同,则11.5g气体A和8gO2 的物质的量相同,根据M=
计算氧气的物质的量,同温同压下,二者体积相同,则11.5g气体A和8gO2 的物质的量相同,根据M=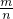 计算气体A的摩尔质量,据此判断气体A的相对分子质量.
计算气体A的摩尔质量,据此判断气体A的相对分子质量.
解答:8gO2 的物质的量为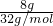 =0.25mol,
=0.25mol,
同温同压下,二者体积相同,则11.5g气体A和8gO2 的物质的量相同,即气体A的物质的量为0.25mol.
所以气体A的摩尔质量为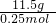 =46g/mol.
=46g/mol.
所以该气体的相对分子质量为46.
故选:A.
点评:考查阿伏伽德罗定律及推论的计算,难度不大,注意相对分子质量的计算方法,根据同温同压下,体积之比等于物质的量之比,判断气体的物质的量是解题关键.
分析:根据n=
 计算氧气的物质的量,同温同压下,二者体积相同,则11.5g气体A和8gO2 的物质的量相同,根据M=
计算氧气的物质的量,同温同压下,二者体积相同,则11.5g气体A和8gO2 的物质的量相同,根据M=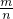 计算气体A的摩尔质量,据此判断气体A的相对分子质量.
计算气体A的摩尔质量,据此判断气体A的相对分子质量.解答:8gO2 的物质的量为
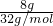 =0.25mol,
=0.25mol,同温同压下,二者体积相同,则11.5g气体A和8gO2 的物质的量相同,即气体A的物质的量为0.25mol.
所以气体A的摩尔质量为
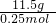 =46g/mol.
=46g/mol.所以该气体的相对分子质量为46.
故选:A.
点评:考查阿伏伽德罗定律及推论的计算,难度不大,注意相对分子质量的计算方法,根据同温同压下,体积之比等于物质的量之比,判断气体的物质的量是解题关键.

练习册系列答案
相关题目