��Ŀ����
����Ŀ��CO2������Դ�������ǻ���������峵��ȵ���⣬
(1)��FeO���£���CO2Ϊԭ����ȡ̿��(C)��̫���ܹ�����ͼ1��ʾ��
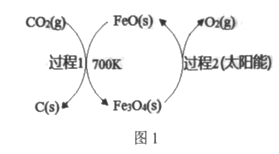
��֪���ٹ���1����lmolC(s)�ķ�Ӧ��Ϊ��H1��
�ڹ���2��Ӧ��Fe3O4(s)![]() 3FeO(s)+l/2O2(g) ��H2��
3FeO(s)+l/2O2(g) ��H2��
������CO2Ϊԭ����ȡ̿���ܷ�Ӧ���Ȼ�ѧ����ʽΪ____________�����÷�Ӧ�ġ�S<0�����ж�
�÷�Ӧ�Ƿ�Ϊ�Է���Ӧ��˵������___________________��
(2)��CO2Ϊԭ�Ͽ��Դ�����ϳɵ�̼ϩ��������CO2�ϳ���ϩ�ķ�Ӧ����ʽΪ��2CO2(g)+6H2(g) ![]() C2H4(g)+4H2O(g) ��H3���ڳ�ѹ�£��� FeCoMnK/BeO ����������n(CO2)�� n(H2)=l��3(�����ʵ���Ϊ4amol)��Ͷ�ϱȳ����ܱ������з�����Ӧ������¶ȶ�CO2��ƽ��ת���ʺʹ�����Ч��Ӱ�������ͼ2��ʾ��
C2H4(g)+4H2O(g) ��H3���ڳ�ѹ�£��� FeCoMnK/BeO ����������n(CO2)�� n(H2)=l��3(�����ʵ���Ϊ4amol)��Ͷ�ϱȳ����ܱ������з�����Ӧ������¶ȶ�CO2��ƽ��ת���ʺʹ�����Ч��Ӱ�������ͼ2��ʾ��

������˵������ȷ����______________��
A. ��H3<0��ƽ�ⳣ����KM >KN
B.����ԭ�����ı��������ƽ��ת������Ӱ��
C.������ϩ�����ʣ�v(M)�п���С��v(N)
D.��Ͷ�ϱȸ�Ϊn(CO2)��n(H2)=1��2���������CO2��ƽ��ת����
E.��Ͷ�ϱȲ��䣬�¶�Խ�ͣ���Ӧһ��ʱ���CO2��ת����Խ��
��250���£�������Ӧ��ƽ��ʱ�������ΪVL������¶��¸÷�Ӧ��ƽ�ⳣ��Ϊ___________(�ú�a��V�Ĵ���ʽ��ʾ����
��ij�¶��£�n(C2H4)��ʱ��(t)�ı仯����������ͼ3��ʾ������������ͬʱ�������������Ϊ��һ�룬����0��t1ʱ��n(C2H4)��ʱ��(t)�ı仯�������ߡ�______
(3)��ϡ����Ϊ�������Һ������̫���ܿɽ�CO2���ת��Ϊ��̼ϩ�����������ɱ�ϩʱ�������ĵ缫��ӦΪ______________��
���𰸡� CO2(g)=C(s)+O2(g) ��H1+2��H2 �÷�ӦΪ���Է���Ӧ����Ϊ�÷�Ӧ�Ħ�H>0����S<0 DE K=V3/1.56a3��Kp=[3.253/1000��1.56] MPa-3 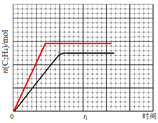 3CO2+18e-+18H+��CH2=CH-CH3+6H2O
3CO2+18e-+18H+��CH2=CH-CH3+6H2O
�����������������(1).�ٹ���1����lmolC(s)�ķ�Ӧ��Ϊ��H1����֪����1���Ȼ�ѧ����ʽΪ![]() ��H1 ���ڹ���2��Ӧ��Fe3O4(s)
��H1 ���ڹ���2��Ӧ��Fe3O4(s)![]() 3FeO(s)+l/2O2(g) ��H2 �����ݸ�˹���ɼ�����CO2Ϊԭ����ȡ̿���ܷ�Ӧ���ʱ䡣���ݷ�Ӧ�����оݷ�����Ӧ�ܷ��Է����У�(2) ������ͼ2��֪�����¶�����CO2��ƽ��ת���ʼ�С���������¶�ƽ�������ƶ�����������ƽ���ƶ���Ӱ�죻����ͼ2��֪��M������Ĵ�Ч�ʴ���N�������������ı������������CO2��ת����Խ���¶�Խ�ͣ���Ӧ����ԽС��������ͼ2��֪��250���£�CO2��ƽ��ת����Ϊ50%������ ������ʽ������ƽ�ⳣ����������������ͬʱ�������������Ϊ��һ�룬ѹǿ����Ӧ���ʼӿ죬�ﵽƽ���õ�ʱ����٣�����ѹǿƽ�������ƶ�����ϩ��ƽ�����ʵ�������(3)����̫���ܽ�CO2���ת��Ϊ��̼ϩ���������Ƕ�����̼�õ���������ϩ��
3FeO(s)+l/2O2(g) ��H2 �����ݸ�˹���ɼ�����CO2Ϊԭ����ȡ̿���ܷ�Ӧ���ʱ䡣���ݷ�Ӧ�����оݷ�����Ӧ�ܷ��Է����У�(2) ������ͼ2��֪�����¶�����CO2��ƽ��ת���ʼ�С���������¶�ƽ�������ƶ�����������ƽ���ƶ���Ӱ�죻����ͼ2��֪��M������Ĵ�Ч�ʴ���N�������������ı������������CO2��ת����Խ���¶�Խ�ͣ���Ӧ����ԽС��������ͼ2��֪��250���£�CO2��ƽ��ת����Ϊ50%������ ������ʽ������ƽ�ⳣ����������������ͬʱ�������������Ϊ��һ�룬ѹǿ����Ӧ���ʼӿ죬�ﵽƽ���õ�ʱ����٣�����ѹǿƽ�������ƶ�����ϩ��ƽ�����ʵ�������(3)����̫���ܽ�CO2���ת��Ϊ��̼ϩ���������Ƕ�����̼�õ���������ϩ��
������(1).�ٹ���1����lmolC(s)�ķ�Ӧ��Ϊ��H1����֪����1���Ȼ�ѧ����ʽΪ![]() ��H1 ���ڹ���2��Ӧ��Fe3O4(s)
��H1 ���ڹ���2��Ӧ��Fe3O4(s)![]() 3FeO(s)+l/2O2(g) ��H2 �����ݸ�˹���ɢ�+2��������CO2(g)=C(s)+O2(g) ��H1+2��H2���÷�Ӧ�Ħ�H>0����S<0��
3FeO(s)+l/2O2(g) ��H2 �����ݸ�˹���ɢ�+2��������CO2(g)=C(s)+O2(g) ��H1+2��H2���÷�Ӧ�Ħ�H>0����S<0�� ![]() ,���Ը÷�ӦΪ���Է���Ӧ��
,���Ը÷�ӦΪ���Է���Ӧ��
(2) ������ͼ2��֪�����¶�����CO2��ƽ��ת���ʼ�С���������¶�ƽ�������ƶ������ԡ�H3<0��ƽ�ⳣ����KM >KN����A��ȷ��������ƽ���ƶ���Ӱ�죬��B��ȷ��������ͼ2��֪��M������Ĵ�Ч�ʴ���N�㣬M����¶ȵ���M�㣬����v(M)�п���С��v(N)����C��ȷ�����������ı������������CO2��ת����Խ����Ͷ�ϱȸ�Ϊn(CO2)��n(H2)=1��2�����Խ���CO2��ƽ��ת��������D�����¶�Խ�ͣ���Ӧ����Խ������Ӧһ��ʱ���CO2��ת���ʿ��ܽϵͣ���E������������ͼ2��֪��250���£�CO2��ƽ��ת����Ϊ50%��
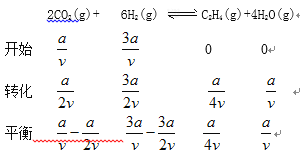
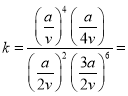 V3/1.56a3 ��
V3/1.56a3 ��
������������ͬʱ�������������Ϊ��һ�룬ѹǿ����Ӧ���ʼӿ죬�ﵽƽ���õ�ʱ����٣�����ѹǿƽ�������ƶ�����ϩ��ƽ�����ʵ���������ͼ��Ϊ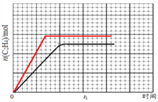 ��
��
(3)����̫���ܽ�CO2���ת��Ϊ��̼ϩ���������Ƕ�����̼�õ���������ϩ�������ĵ缫��ӦΪ3CO2+18e-+18H+��CH2=CH-CH3+6H2O��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ��������X����(��ͨ��)Y��Һ��,���ɳ������������X�����ʵ�����ϵ��ͼ��ʾ,����ͼʾ�������( )

A | B | C | D | |
X | CO2 | HCl | NaOH | AlCl3 |
Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
A. A B. B C. C D. D
