题目内容
铁是人体必须的微量元素,治疗缺铁性贫血
的常见方法是服用补铁药物。“速力菲”(主要成分:
琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁
药物。该药品不溶于水但能溶于人体中的胃酸。某
同学为了检测“速力菲”药片中Fe2+的存在,设计
并进行了如下实验:
(1)试剂1是 。
(2)加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了红色,其可能的原因是 。
(3)在实验中发现放置一段时间,溶液的颜色会逐渐褪去。为了进一步探究溶液褪色的原因,甲、乙、丙三位同学首先进行了猜想:
| 编号 | 猜想 |
| 甲 | 溶液中的+3价Fe又被还原为+2价Fe |
| 乙 | 溶液中的SCN-被过量的氯水氧化 |
| 丙 | 新制的氯水具有漂白性,将该溶液漂白 |
| 编号 | 实验操作 | 预期现象和结论 |
| | | |
(1)稀盐酸(或稀硫酸溶液)(2分)
(2)Fe2+被空气中氧气氧化成Fe3+;(2分)
(其他合理答案也可给分)编号 实验操作 预期现象和结论 ① 取少量褪色后溶液,加入KSCN溶液 如果溶液变红色,说明乙同学的猜想是合理的;如果溶液不变红色,说胆乙同学的猜想是不合理的 或 取少量褪色后溶液,加入FeCl3溶液 如果溶液仍不变红色,说明乙同学的猜想是合理的;如果溶液变红色,说明乙同学的猜想是不合理的
解析

 名校课堂系列答案
名校课堂系列答案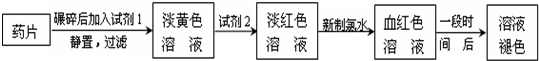
(1)试剂1是
(2)加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了红色,其可能的原因是
(3)在实验中发现放置一段时间,溶液的颜色会逐渐褪去.为了进一步探究溶液褪色的原因,甲、乙、丙三位同学首先进行了猜想:
| 编号 | 猜想 |
| 甲 | 溶液中的+3价Fe又被还原为+2价Fe |
| 乙 | 溶液中的SCN-被过量的氯水氧化 |
| 丙 | 新制的氯水具有漂白性,将该溶液漂白 |
| 编号 | 实验操作 | 预期现象和结论 |
铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。
某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:

(1)试剂1是 ,加入新制氯水后溶液中发生的离子反应方程式是: , ;
(2)加入KSCN溶液后,在未加新制氯水的情况下,溶液中也产生了红色,其可能的原因是 ;
(3)在实验中发现放置一段时间,溶液的颜色会逐渐褪去。为了进一步探究溶液褪色的原因,甲、乙、丙三位同学首先进行了猜想:
|
编号 |
猜 想 |
|
甲 |
溶液中的+3价Fe又被还原为+2价Fe |
|
乙 |
溶液中的SCN-被过量的氯水氧化 |
|
丙 |
新制的氯水具有漂白性,将该溶液漂白 |
基于乙同学的猜想,请设计实验方案,验证乙同学的猜想是否正确。写出有关的实验操作、预期现象和结论。(不一定填满,也可以补充)
|
编号 |
实验操作 |
预期现象和结论 |
|
① |
|
|
|
|
|
|
|
|
|
|