题目内容
普通玻璃中Na2SiO3∶CaSiO3∶SiO2=1∶1∶4(物质的量之比)。
(1)若以aNa2O·bCaO·mSiO2表示此玻璃的组成,则a∶b∶m= 。
(2)若要制备1000kg上述玻璃,需要原料各多少千克?共可产生标准状况下的CO2气体多少升?
(1)若以aNa2O·bCaO·mSiO2表示此玻璃的组成,则a∶b∶m= 。
(2)若要制备1000kg上述玻璃,需要原料各多少千克?共可产生标准状况下的CO2气体多少升?
(1)1∶1∶6
(2)m(Na2CO2):221.8kg m(SiO2):209.2kg m(SiO2):753.1kg V(CO2):9.37×104L
(2)m(Na2CO2):221.8kg m(SiO2):209.2kg m(SiO2):753.1kg V(CO2):9.37×104L
(1)根据原子个数相等的原则,Na2SiO3·CaSiO3·4SiO2等同于Na2O·CaO·6SiO2,即a∶b∶m=1∶1∶6。
(2)制造玻璃的原料是Na2CO3、CaCO3和SiO2,根据反应原理:Na2CO3+SiO2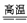 Na2SiO3+CO2↑,CaCO3+SiO2
Na2SiO3+CO2↑,CaCO3+SiO2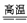 CaSiO3+CO2↑得
CaSiO3+CO2↑得
Na2O·CaO·6SiO2~Na2CO3~CaCO3~6SiO2~2CO2
478g 1mol 1mol 6mol 2mol
1000×103g x x 6x 2x
x=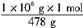 =2092mol
=2092mol
m(Na2CO3)=2092mol×106g·mol-1×10-3kg·g-1=221.8kg;
m(CaCO3)=2092mol×100g·mol-1×10-3kg·g-1=209.2kg;
m(SiO2)=2092mol×6×60g·mol-1×10-3kg·g-1=753.1kg;
V(CO2)=2092mol×2×22.4L·mol-1=9.37×104L。
CO2体积的另一种求法:
制1000kg玻璃需原料:221.8kg+209.2kg+753.1kg=1184.1kg,两者的质量之差就是放出CO2的质量:
V(CO2)=(1184.1-1000)kg×103g·kg-1 44g·mol-1×22.4L·mol-1=9.37×104L。
(2)制造玻璃的原料是Na2CO3、CaCO3和SiO2,根据反应原理:Na2CO3+SiO2
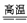 Na2SiO3+CO2↑,CaCO3+SiO2
Na2SiO3+CO2↑,CaCO3+SiO2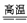 CaSiO3+CO2↑得
CaSiO3+CO2↑得Na2O·CaO·6SiO2~Na2CO3~CaCO3~6SiO2~2CO2
478g 1mol 1mol 6mol 2mol
1000×103g x x 6x 2x
x=
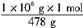 =2092mol
=2092molm(Na2CO3)=2092mol×106g·mol-1×10-3kg·g-1=221.8kg;
m(CaCO3)=2092mol×100g·mol-1×10-3kg·g-1=209.2kg;
m(SiO2)=2092mol×6×60g·mol-1×10-3kg·g-1=753.1kg;
V(CO2)=2092mol×2×22.4L·mol-1=9.37×104L。
CO2体积的另一种求法:
制1000kg玻璃需原料:221.8kg+209.2kg+753.1kg=1184.1kg,两者的质量之差就是放出CO2的质量:
V(CO2)=(1184.1-1000)kg×103g·kg-1 44g·mol-1×22.4L·mol-1=9.37×104L。

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目