题目内容
下表是常温下的五种溶液,下列有关叙述中正确的是( )
A.表中五种溶液,其中①~④由水电离出的c(H+):②=④>①=③
B.在⑤中加入适量④至溶液呈中性,所得溶液:c(Cl-)>c(Na+)
C.分别将①~④加水稀释至原溶液体积的100倍后溶液的pH:①>②>③>④
D.将①、④两种溶液等体积混合所得溶液:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
| | ① | ② | ③ | ④ | ⑤ |
| 溶液 | 氨水 | 氢氧化钠 | 醋酸 | 盐酸 | 醋酸钠 |
| pH | 11 | 11 | 3 | 3 | 8.3 |
B.在⑤中加入适量④至溶液呈中性,所得溶液:c(Cl-)>c(Na+)
C.分别将①~④加水稀释至原溶液体积的100倍后溶液的pH:①>②>③>④
D.将①、④两种溶液等体积混合所得溶液:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
D
试题分析:A、酸或碱抑制水的电离,且溶液中氢离子或氢氧根离子浓度越高抑制程度越大。能水解的盐促进水的电离。因此根据表中数据可知①~④由水电离出的c(H+):②=④=①=③,A不正确;B、根据电荷守恒可知c(H+)+ c(Na+)=c(Cl-)+c(OH-)+c(CH3COO-),溶液显中性,则c(OH-)=c(H+),所以c(Na+)=c(Cl-)+c(CH3COO-),即c(Cl-)<c(Na+),B不正确;C、氢氧化钠和盐酸是强电解质,完全电离。氨水和醋酸是弱碱、弱酸,部分电离,所以分别将①~④加水稀释至原溶液体积的100倍后溶液的pH:①>②>④>③,C不正确;D、将①、④两种溶液等体积混合后氨水过量,溶液显碱性,则所得溶液:c(NH4+)>c(Cl-)>c(OH-)>c(H+),D正确,答案选D。

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
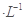 NaOH溶液中逐滴加入。0.2mol
NaOH溶液中逐滴加入。0.2mol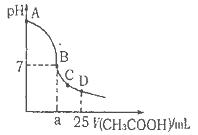
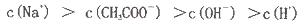
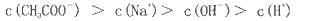
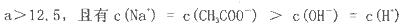
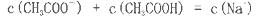
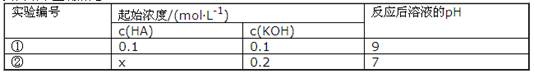
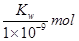 ·L-1
·L-1 0.1mol·L-l
0.1mol·L-l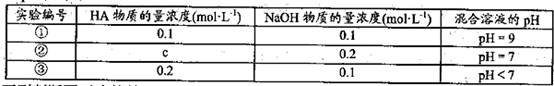
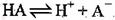
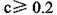
 Co2+(粉红色)+4Cl-,向氯化钴稀溶液中加入一定量的浓盐酸,溶液的颜色变化是
Co2+(粉红色)+4Cl-,向氯化钴稀溶液中加入一定量的浓盐酸,溶液的颜色变化是