题目内容
X、Y和Z是短周期元素组成的三种单质,X的组成元素是第三周期原子半径最大的元素;Y和Z均由元素R组成,Y由两个原子组成,R最外层电子数是内层电子数的3倍,下列推断正确的是( )
| A、Y和Z互为同位素 | B、X和Y能化合成两种化合物 | C、X和Y化合的产物中一定不含有共价键 | D、X离子比R的离子半径小 |
分析:X、Y和Z是短周期元素组成的三种单质,X的组成元素是第三周期原子半径最大的元素,则X为Na;R最外层电子数是内层电子数的3倍,则R原子只能有2个电子层,最外层电子数为6,则R为O元素,Y和Z均由元素R组成,则Y、Z互为同素异形体,Y由两个原子组成,则Y为O2、Z为O3,据此解答.
解答:解:X、Y和Z是短周期元素组成的三种单质,X的组成元素是第三周期原子半径最大的元素,则X为Na;R最外层电子数是内层电子数的3倍,则R原子只能有2个电子层,最外层电子数为6,则R为O元素,Y和Z均由元素R组成,则Y、Z互为同素异形体,Y由两个原子组成,则Y为O2、Z为O3,
A.同位素是质子数相同,中子数不同的同种原子,O2、O3是氧元素组成的结构不同的单质,二者互为同素异形体,故A错误;
B.Na和氧气反应可以生成Na2O、Na2O2,故B正确;
C.X和Y化合可以得到过氧化钠,过氧化钠含有共价键,故C错误;
D.Na+、O2-电子层结构相同,核电荷数越大离子半径越小,故离子半径Na+<O2-,故D正确,
故选:BD.
A.同位素是质子数相同,中子数不同的同种原子,O2、O3是氧元素组成的结构不同的单质,二者互为同素异形体,故A错误;
B.Na和氧气反应可以生成Na2O、Na2O2,故B正确;
C.X和Y化合可以得到过氧化钠,过氧化钠含有共价键,故C错误;
D.Na+、O2-电子层结构相同,核电荷数越大离子半径越小,故离子半径Na+<O2-,故D正确,
故选:BD.
点评:本题考查结构性质位置关系应用,涉及元素化合物推断、离子半径比较、元素化合物结构与性质等,比较基础,注意基础知识的理解掌握,注意掌握半径比较规律.

练习册系列答案
相关题目
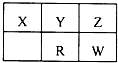 短周期元素X、Y、Z、R和W在元素周期表的位置如图所示,其中W元素族序数等于周期序数的2倍.则下列说法正确的是( )
短周期元素X、Y、Z、R和W在元素周期表的位置如图所示,其中W元素族序数等于周期序数的2倍.则下列说法正确的是( )| A、原子半径从小到大:X<Y<R<W | B、Z、W元素与X均可以形成AB2型化合物 | C、X有多种同素异形体,而Z不存在同素异形体 | D、Z的氢化物稳定性大于W的氢化物稳定性,是因为Z的氢化物分子间存在氢键 |
在当代,能源同信息、材料一起构成了现代文明的三大支柱。碳元索是能源领域的主角之一,材料和医学领域等也与碳元素息息相关。
(1)X、Y、Z是短周期中除碳外的非金属元素,它们在周期表中分处于三个不同的周期且原子序数依次增大;X分别与Y和Z以原子个数比1:1相结合时均可形成18电子的分子。请写出三个符合下列条件的化学方程式:
 a.所有的反应物和生成物都由×、Y、Z及碳四种元素中的一种或两种组成;
a.所有的反应物和生成物都由×、Y、Z及碳四种元素中的一种或两种组成;
b.反应物中有单质参加且只有一种,三个反应中的单质不同。
(2)由元素X、Y及碳组成的化合物A的球棍结构如右图:
| 利川A、 |
利用A、O2和KOH可组成燃料电池,则在该电池正极发生反应的物质是 ,负极的电极反应式为 ;
![]()
![]()
(3)有机玻璃 是由A和通过和_______反应合成的,该合成反应第一步的化学方程式为 。物质结构和元素周期律;化学与材料的制造、应用;