��Ŀ����
X��Y��Z��WΪ��ԭ��������С�������е����ֶ����ڵ�Ԫ�أ�����Y��Wλ��ͬһ���壬Z��Wλ��ͬһ���ڣ�Y��������������K���������3����Z��ͬһ�����н�������ǿ��Ԫ�أ�X��������������Z��ͬ����XΪ�ǽ���Ԫ�أ���ش��������⣺
��1��Y��Z��Ԫ�ط��ŷֱ��� �� ��
��2��Z2W�ĵ���ʽ�� ��
��3��Z2Y2��X2Y��Ӧ�Ļ�ѧ����ʽ�ǣ�
��4��Z2WY3��X2WY4��Ӧ�����ӷ���ʽ�ǣ� ��
��1��Y��Z��Ԫ�ط��ŷֱ���
��2��Z2W�ĵ���ʽ��
��3��Z2Y2��X2Y��Ӧ�Ļ�ѧ����ʽ�ǣ�
��4��Z2WY3��X2WY4��Ӧ�����ӷ���ʽ�ǣ�
������X��Y��Z��WΪ��ԭ��������С�������е����ֶ����ڵ�Ԫ�أ�����Y��Wλ��ͬһ���壬��Y���ڵڶ����ڡ�W���ڵ������ڣ�Y��������������K���������3������Y����������Ϊ6����YΪ��Ԫ�أ���WΪ��Ԫ�أ�Z��Wλ��ͬһ���ڣ�Z��ͬһ�����н�������ǿ��Ԫ�أ���ZΪ��Ԫ�أ�XΪ�ǽ���Ԫ�أ���������������Z��ͬ����XΪ��Ԫ�أ��ݴ˽��
����⣺X��Y��Z��WΪ��ԭ��������С�������е����ֶ����ڵ�Ԫ�أ�����Y��Wλ��ͬһ���壬��Y���ڵڶ����ڡ�W���ڵ������ڣ�Y��������������K���������3������Y����������Ϊ6����YΪ��Ԫ�أ���WΪ��Ԫ�أ�Z��Wλ��ͬһ���ڣ�Z��ͬһ�����н�������ǿ��Ԫ�أ���ZΪ��Ԫ�أ�XΪ�ǽ���Ԫ�أ���������������Z��ͬ����XΪ��Ԫ�أ�
��1��������������֪��YΪOԪ�ء�ZΪNa���ʴ�Ϊ��O��Na��
��2��ZΪ��Ԫ�ء�WΪ��Ԫ�أ������γ�Na2S��Na2S�����ӻ��������������������ӹ��ɣ�����ʽΪ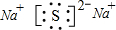 ���ʴ�Ϊ��
���ʴ�Ϊ��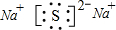 ��
��
��3��Z2Y2��X2Y�ֱ�ΪNa2O2��H2O������������ˮ��Ӧ����������������������Ӧ���ӷ���ʽΪ2Na2O2+2H2O=4Na++4OH-+O2����
�ʴ�Ϊ��2Na2O2+2H2O=4Na++4OH-+O2����
��4��Z2WY3��X2WY4�ֱ�ΪNa2SO3��H2SO4�����߷�Ӧ���������ơ�SO2��ˮ����Ӧ�Ļ�ѧ����ʽΪ��Na2SO3+H2SO4=Na2SO4+SO2��+H2O����Ӧʵ��Ϊ��SO32-+2H+=SO2��+H2O���ʴ�Ϊ��SO32-+2H+=SO2��+H2O��
��1��������������֪��YΪOԪ�ء�ZΪNa���ʴ�Ϊ��O��Na��
��2��ZΪ��Ԫ�ء�WΪ��Ԫ�أ������γ�Na2S��Na2S�����ӻ��������������������ӹ��ɣ�����ʽΪ
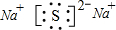 ���ʴ�Ϊ��
���ʴ�Ϊ��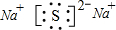 ��
����3��Z2Y2��X2Y�ֱ�ΪNa2O2��H2O������������ˮ��Ӧ����������������������Ӧ���ӷ���ʽΪ2Na2O2+2H2O=4Na++4OH-+O2����
�ʴ�Ϊ��2Na2O2+2H2O=4Na++4OH-+O2����
��4��Z2WY3��X2WY4�ֱ�ΪNa2SO3��H2SO4�����߷�Ӧ���������ơ�SO2��ˮ����Ӧ�Ļ�ѧ����ʽΪ��Na2SO3+H2SO4=Na2SO4+SO2��+H2O����Ӧʵ��Ϊ��SO32-+2H+=SO2��+H2O���ʴ�Ϊ��SO32-+2H+=SO2��+H2O��
���������⿼��λ�ýṹ���ʵ����ϵ�����û�ѧ����ȣ��ǶԻ���֪ʶ���ۺϿ��飬�Ѷ��еȣ�����Ԫ��λ�ù�ϵ���ƶ�Ԫ�������������ǽ���Ĺؼ���

��ϰ��ϵ�д�
 ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�
�����Ŀ
X��Y��Z��Q��WΪ��ԭ��������С�������е����ֶ�����Ԫ�ء���֪����X��Q����ͬһ���壬��ԭ�Ӽ۵����Ų�ʽ��Ϊns2np2����Xԭ�Ӱ뾶С��Q����YԪ���ǵؿ��к�������Ԫ�أ�WԪ�صĵ縺��·С��YԪ�أ���Wԭ�ӵļ۵����Ų�ʽ�У�p�����ֻ��1��δ�ɶԵ��ӣ���ZԪ�صĵ��������ݼ��±���kJ��mol-1��
|
I1 |
I2 |
I3 |
I4 |
�� |
|
496 |
4562 |
6912 |
9540 |
�� |
��ش�
��1��XY2���ӵĿռ乹��Ϊ ��
��2��QX�ľ���ṹ����ʯ�����ƣ�������ڵ��������� ��
��3������ZW���۵�Ⱦ���XW4���Ըߵ�ԭ���� ��
��4��XY2�ڸ��¸�ѹ�����γɵľ�����ͼ��ʾ���þ������������ ��ѡ����ӡ�����ԭ�ӡ��������ӡ���������©�壬�þ�����Xԭ�ӵ��ӻ���ʽΪ___ ��

��5��������MO�ĵ���������QX����ȣ���MΪ ������Ԫ�ط��ţ���MO�����������²��ϣ��侧��ṹ��ZW����ṹ���ƣ�MO���۵��CaO�ĸߣ���ԭ���� ��





