题目内容
某元素的最外层电子数为2,价电子数为5,并且是同族中原子序数最小的元素,关于该元素的判断错误的是( )
| A、电子排布式为:1s22s22p63s23p63d34s2 |
| B、该元素为V |
| C、元素为ⅢB族元素 |
| D、该元素属于过渡元素 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:某元素的最外层电子数为2,价电子数为5,说明最外层电子数和价电子数不相等,应存在d能级电子,并且是同族中原子序数最小的元素,则价电子排布为3d34s2,电子排布式为1s22s22p63s23p63d34s2,以此解答该题.
解答:
解:某元素的最外层电子数为2,价电子数为5,说明最外层电子数和价电子数不相等,应存在d能级电子,并且是同族中原子序数最小的元素,则价电子排布为3d34s2,电子排布式为1s22s22p63s23p63d34s2,为第4周期ⅤB族元素,为V元素,属于过渡元素,故ABD正确、C错误,
故选C.
故选C.
点评:本题考查结构与位置关系等,侧重于原子核外电子排布的考查,难度中等,推断元素是关键,注意基础知识掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
化合物X(分子式为C2H6O)具有如下性质:X+Na→慢慢产生气泡;X+乙→有香味产物Y.以下判断正确的是( )
| A、X的结构简式为CH3OCH3 |
| B、香味产物分子式为C4H10O3 |
| C、x可由乙烯通过加成反应制得 |
| D、X、Y和乙酸均能与烧碱反应 |
现有C2H2、CH3CHO、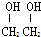 三种蒸汽的混合物,已知含C量为a%,则氢的含量为( )
三种蒸汽的混合物,已知含C量为a%,则氢的含量为( )
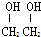 三种蒸汽的混合物,已知含C量为a%,则氢的含量为( )
三种蒸汽的混合物,已知含C量为a%,则氢的含量为( )A、
| ||||
B、
| ||||
C、
| ||||
| D、无法计算 |
有5种粒子,它们分别是
K+,
Ar,
K,
Ca2+,
Ca,则它们所属元素的种类有( )
| 40 |
| 19 |
| 40 |
| 18 |
| 40 |
| 19 |
| 40 |
| 20 |
| 41 |
| 20 |
| A、2种 | B、3种 | C、4种 | D、5种 |
下列有关胶体的说法不正确的是( )
| A、向Fe(OH)3胶体中滴加过量的稀硫酸,会产生红褐色沉淀 |
| B、葡萄糖注射液不能产生丁达尔现象,不属于胶体 |
| C、向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H2O?Al(OH)3(胶体)+3H+ |
| D、在水泥和冶金工厂常用高压电除去大量烟尘,以减少对空气的污染化学在生产和日 |
短周期主族元素X、Y、Z、W的原子序数依次增大,X原子核外最外层电子数是次外层的2倍,Y的氟化物YF3分子中各原子均达到8电子稳定结构,Z是同周期中原子半径最大的元素,W的最高正价为+7价.下列说法正确的是( )
| A、XH4的沸点比YH3高 |
| B、X与W形成的化合物和Z与W形成的化合物的化学键类型相同 |
| C、元素W的最高价氧化物对应水化物的酸性比Y的强 |
| D、X与Y形成的化合物的熔点可能比金刚石高 |
下列说法正确的是( )
| A、向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色 |
| B、欲除去氯气中少量的氯化氢气体,可将此混合气体通过盛饱和食盐水的洗气瓶 |
| C、将AgNO3溶液滴入某溶液中,若出现沉淀,则说明溶液中含有Cl- |
| D、将氯水滴入碳酸钠溶液中,无明显现象出现 |
下列各项反应对应的图象错误的是( )
A、 将饱和FeCl3溶液滴入沸水中制备Fe(OH)3胶体 |
B、 将稀盐酸逐滴加入一定量偏铝酸钠溶液中 |
C、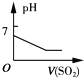 将二氧化硫逐渐通入一定量氯水中 |
D、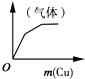 将铜粉逐渐加入一定量浓硝酸中 |
下列符号所代表的微粒不影响水的电离平衡的是( )
A、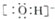 |
| B、HCO3- |
C、 |
D、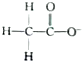 |