题目内容
(共14分)右图中,A为空气中常见的气体单质、B、C、E是金属单质,D为非金属单质。已知:①I是一种常见的温室气体,E原子核内有12个质子②反应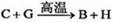 能放出大量的热,该反应曾应用于铁轨的焊接;回答下列问题:
能放出大量的热,该反应曾应用于铁轨的焊接;回答下列问题:
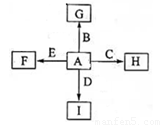
(1)分别写出F、G、H、I的化学式
F G H I
(2)书写下列化学方程式
 ;
;
(3)C与NaOH溶液反应的化学方程式为 ,
反应后溶液与过量化合物I反应的化学方程式为 ;
⑷ 1.6gG溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需的铜粉的质量为:
(提示 :2FeCl3 + Cu ==2FeCl2+ CuCl2 );
⑴ MgO Fe2O3 Al2O3 CO2 (每空1分)
⑵2Al+ Fe2O3 2Fe+ Al2O3 (2分) 2Mg+ CO2===
2Fe+ Al2O3 (2分) 2Mg+ CO2=== == 2MgO + C (2分)
== 2MgO + C (2分)
⑶ 2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑ (2分)
NaAlO2 + CO2 + 2H2O = Al(OH)3↓+ NaHCO3 (2分)
⑷ m(Cu)==0.64 g
【解析】m(Fe2O3)== 1.6 g /160g. -1 ==0.01 mol
Fe2O3 + 6HCl == 2FeCl3 + 3H2O 2FeCl3 + Cu ==2FeCl2+ CuCl2
0.01mol 0.02 mol 0.02mol 0.01 mol
m(Cu)== 0.01 mol×64 g/mol == 0.64 g

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科学的发展有一个不断深化的过程。人们对有机化合物的认识同样是这样。
(1)1828年,德国化学家武勒(F?WOhler)冲破了生命力学说的束缚,在实验室里将无机物氰酸铵(NH4CNO)溶液蒸发,得到了有机物尿素[CO(NH2)2]。
|
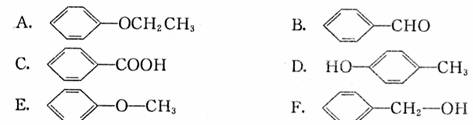
互为同分异构体的是
|
它不能解释下列 事实
(填入编号)
a.苯不能使溴水褪色
b.苯能与H2 发生加成反应
c.溴苯没有同分异构体
d.邻二溴苯只有一种
将苯与浓硫酸和硝酸混合共热并保存50℃―60℃的温度,可以生成硝基苯。反应后的仪器中有硝基苯、苯和残酸,为得到纯净的硝基苯,要进行中和、水洗,其目的是 ;已知苯的沸点是80℃,硝基苯的沸点是210.9℃,将苯与基苯分离开的实验操作是 。
(3)糖类又称碳水化合物,这是因为过去发现的糖类太多可以用通式Cn(H2O)m来表示。实际上很多符合通式为Cn(H2O)m的化合物并不属于糖类,写出两种符合通式Cn(H2O)m而不属于糖类的有机化合物的结构简式 。
(4)1830年,德国化学家李比希发展了碳、氢分析法,为有机化合物的定量分析打下了基础。某含C、H、O三种元素的未知物,经燃烧实验测定该未知物中碳的质量分数为52.16%,氢的质量分数为13.14%,则A的分子式为 。
A为有关物质存在如下转化关系,B是当今世界产量最大的塑料,广泛用于食品、医药、衣物、化肥等的包装。
![]()
写出下列反应化学方程式
①
。
② 。
 能放出大量的热,该反应曾应用于铁轨的焊接;回答下列问题:
能放出大量的热,该反应曾应用于铁轨的焊接;回答下列问题: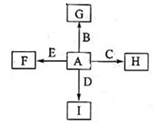
 ;
;