题目内容
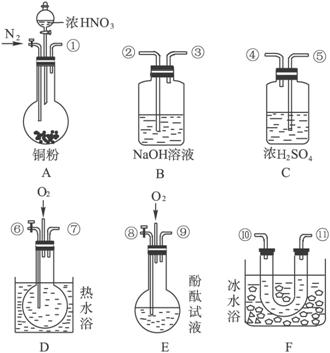
用如下图所示气体发生装置可以制取SO2(两种方法)和氯化氢(两种方法)气体,分别写出有关化学反应的化学方程式。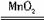
(1)制SO2(氧化还原反应) ;制SO2(复分解反应) 。
(2)制HCl的化学方法: ;制HCl的物理方法:烧瓶中盛 ,分液漏斗中盛 。
(3)如果撤去酒精灯,此装置可用于制H2、CO2、H2S及O2,如果用于制O2,烧瓶中盛 ,分液漏斗中盛 ,所发生反应的化学方程式为 。
解析:(1)浓H2SO4具有强氧化性,与Cu或木炭粉在加热条件下反应被还原为SO2,因此可用浓H2SO4的氧化性来制取SO2。H2SO3不稳定,在加热条件下易分解,可通过强酸制弱酸得到H2SO3,再加热使其分解制SO2。
(2)实验室制取HCl是利用浓H2SO4的高沸点性,NaCl与浓H2SO4在加热条件下制得HCl气体。物理方法制HCl是利用了浓盐酸的挥发性,浓H2SO4吸水有利于HCl的溢出(注意浓H2SO4与其他液体混合时一般是向其他液体中慢慢滴加浓H2SO4)。
(3)实验室制O2是固体与固体在加热条件下的反应,而题目要求撤去酒精灯,因此不能用实验室方法来制取。本题可利用H2O2的不稳定性,易分解来制取O2。
答案:(1)Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
Na2SO3+H2SO4 ![]() Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O
(2)NaCl+H2SO4(浓) ![]() NaHSO4+HCl↑
NaHSO4+HCl↑
浓盐酸 浓H2SO4
(3)MnO2 H2O2 2H2O2 ![]() 2H2O+O2↑
2H2O+O2↑

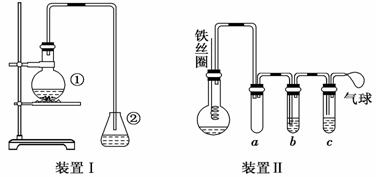
(14分)用如下图所示装置可以完成一系列实验(图中夹持装置已略去)

请回答下列问题:
Ⅰ.若气体a是Cl2,装置A、B、C中的试剂依次为: FeCl2溶液、淀粉KI溶液、石蕊溶液。
装置 A B C D
试剂 FeCl2溶液 淀粉KI溶液 石蕊溶液
现象 溶液由浅绿色变为棕黄色
离子方程式
II.若气体a是SO2,装置A、B、C中的试剂依次为:品红溶液、酸性高锰酸钾溶液、氢硫酸(硫化氢的水溶液)。
|
装置 |
A |
B |
C |
|
试剂 |
品红溶液 |
酸性高锰酸钾溶液 |
硫化氢的水溶液 |
|
现象 |
|
紫色退去 |
|
|
体现SO2的性质 |
|
|
氧化性 |
(1)写出C中发生反应的化学方程式 。
(2)D装置中用氢氧化钠溶液来吸收SO2,为了防止倒吸,应该选用下列装置中的 (填序号)。