题目内容
【题目】500mLKNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0mo/L,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是
A. 原混合溶液中c(K+)为2mol/L B. 上述电解过程中共转移2mol电子
C. 电解得到的Cu的物质的量为0.5mol D. 电解后溶液中c(H+)为2mol/L
【答案】A
【解析】电解硝酸钾和硝酸铜混合溶液时,阳极上氢氧根离子放电生成氧气,阴极上先铜离子放电生成铜单质,当铜离子完全析出时,氢离子放电生成氢气,气体的物质的量= ![]() =1mol;每生成1mol氧气转移4mol电子,每生成1mol氢气转移2mol电子,每生成1mol铜转移2mol电子,所以根据转移电子守恒得铜的物质的量=
=1mol;每生成1mol氧气转移4mol电子,每生成1mol氢气转移2mol电子,每生成1mol铜转移2mol电子,所以根据转移电子守恒得铜的物质的量= ![]() =1mol,则铜离子的物质的量浓度=
=1mol,则铜离子的物质的量浓度= ![]() =2mol/L,根据电荷守恒得钾离子浓度=6mol/L-2mol/L×2=2mol/L,A.根据分析知,原混合溶液中c(K+)为2molL-1,选项A正确;B.转移电子的物质的量=1mol×4=4mol,选项B错误;C.根据以上分析知,铜的物质的量为1mol,选项C错误;D.当电解硝酸铜时溶液中生成氢离子,当电解硝酸钾溶液时,实际上是电解水,所以电解后氢离子的物质的量为氧气的4倍,为1mol×4=4mol,则氢离子浓度=
=2mol/L,根据电荷守恒得钾离子浓度=6mol/L-2mol/L×2=2mol/L,A.根据分析知,原混合溶液中c(K+)为2molL-1,选项A正确;B.转移电子的物质的量=1mol×4=4mol,选项B错误;C.根据以上分析知,铜的物质的量为1mol,选项C错误;D.当电解硝酸铜时溶液中生成氢离子,当电解硝酸钾溶液时,实际上是电解水,所以电解后氢离子的物质的量为氧气的4倍,为1mol×4=4mol,则氢离子浓度= ![]() =8mol/L,选项D错误。答案选A。
=8mol/L,选项D错误。答案选A。

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案【题目】
石墨、石墨烯及金刚石是碳的同素异形体。
(1) 以Ni—Cr—Fe 为催化剂,一定条件下可将石墨转化为金刚石。基态Fe原子未成对电子数为____________。设石墨晶体中碳碳键的键长为a m,金刚石晶体中碳碳键的键长为bm,则a_____b(填“>”、“<”或“=”),原因是_______________________________。
(2)比较下表碳卤化物的熔点,分析其熔点变化规律的原因是____________。
CCl4 | CBr4 | CI4 | |
熔点/℃ | -22.92 | 48.4(α型) | 168(分解) |
(3) 金、铜、锌等金属或合金常用作化学气相沉积法获取石墨烯的催化剂。左下表是铜与锌的部分电离能数据,对于“I1铜小于锌,而I2铜却大于锌”的事实,原因是_________________。
电离能/kJ·mol-1 | I1 | I2 |
铜 | 746 | 1958 |
锌 | 906 | 1733 |
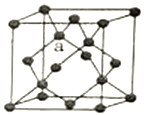
(4)金刚石的晶胞如上图所示。已知ZnS晶胞与金刚石晶胞微粒排列方式相同,若图中a为Zn2+,则S2-处于ZnS晶胞中的位置为___________________________。
(5)石墨烯中部分碳原子被氧化后,转化为氧化石墨烯。

①在图乙所示的氧化石墨烯中,取sp3杂化形式的原子有_________________(填元素符号);
②石墨烯转化为氧化石墨烯时,1号C 与相邻C原子间键能的变化是_____________(填“变大”、“ 变小”或“不变”)。
(6)石墨烯具有很大的比表面积,可望用于制超级电容器。若石墨烯中碳碳键的键长为am,12 g单层石墨烯单面的理论面积约为___________m2(列出计算式即可)。