题目内容
 用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.(1)由上述实验现象所得到的过氧化钠跟水反应的结论是:
①有氧气生成;②反应过程中有
(2)Na2O2跟水反应的化学方程式为
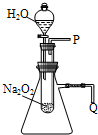
(3)某研究性学习小组拟用右图所示装置(气密性良好)进行实验,以证明上述实验结论.验证第①条结论的实验操作及现象是:向试管中滴入水,
(4)向试管中加水至固体完全溶解且不再有气泡生成后,取出试管,向试管中滴入酚酞试液并振荡,现象为
分析:(1)脱脂棉剧烈燃烧起来,说明该反应中有氧气放出其该反应为放热反应;
(2)过氧化钠与水反应生成氢氧化钠和氧气,据此写出反应的化学方程式;过氧化钠的化合价为-1价,该反应中过氧化钠既是氧化剂,也是还原剂;
(3)根据实验室中常用的检验氧气的方法进行解答;
(4)反应有氢氧化钠生成,溶液显示碱性,同时反应中有双氧水生成,实验室具有漂白性,据此进行解答.
(2)过氧化钠与水反应生成氢氧化钠和氧气,据此写出反应的化学方程式;过氧化钠的化合价为-1价,该反应中过氧化钠既是氧化剂,也是还原剂;
(3)根据实验室中常用的检验氧气的方法进行解答;
(4)反应有氢氧化钠生成,溶液显示碱性,同时反应中有双氧水生成,实验室具有漂白性,据此进行解答.
解答:解:(1)根据反应现象可知,该反应为放热反应,放出的热量时脱脂棉燃烧,反应生成的氧气时燃烧更剧烈,
故答案为:放出大量的热;
(2)过氧化钠与水反应的化学方程式为:2Na2O2+2H2O═4NaOH+O2↑,过氧化钠的化合价为-1价,在反应中过氧化钠的-1价的O化合价升高被氧化成氧气,同时-1价的O被氧化成-1价的O,所以氧化剂、还原剂但是过氧化钠,
故答案为:2Na2O2+2H2O═4NaOH+O2↑; Na2O2;
(3)检验过氧化钠与水反应有氧气放出,可以将带火星的木条放在P口处,木条会复燃,证明反应中有氧气产生,
故答案为:将带火星的木条放在P口处,木条复燃;
(4)向试管中加水至固体完全溶解且不再有气泡生成后,取出试管,向试管中滴入酚酞试液并振荡,由于溶液为碱性溶液,所以滴入酚酞后溶液变成红色,又由于Na2O2与水反应可生成H2O2,H2O2具有强氧化性和漂白性,所以红色的溶液会褪色,所以现象为:溶液先变红后褪色,
故答案为:溶液先变红后褪色.
故答案为:放出大量的热;
(2)过氧化钠与水反应的化学方程式为:2Na2O2+2H2O═4NaOH+O2↑,过氧化钠的化合价为-1价,在反应中过氧化钠的-1价的O化合价升高被氧化成氧气,同时-1价的O被氧化成-1价的O,所以氧化剂、还原剂但是过氧化钠,
故答案为:2Na2O2+2H2O═4NaOH+O2↑; Na2O2;
(3)检验过氧化钠与水反应有氧气放出,可以将带火星的木条放在P口处,木条会复燃,证明反应中有氧气产生,
故答案为:将带火星的木条放在P口处,木条复燃;
(4)向试管中加水至固体完全溶解且不再有气泡生成后,取出试管,向试管中滴入酚酞试液并振荡,由于溶液为碱性溶液,所以滴入酚酞后溶液变成红色,又由于Na2O2与水反应可生成H2O2,H2O2具有强氧化性和漂白性,所以红色的溶液会褪色,所以现象为:溶液先变红后褪色,
故答案为:溶液先变红后褪色.
点评:本题考查了过氧化钠的化学性质,题目难度中等,注意掌握钠及其化合物的性质,熟练掌握过氧化钠与水、二氧化碳反应的化学方程式,明确检验氧气的方法.

练习册系列答案
相关题目




