题目内容
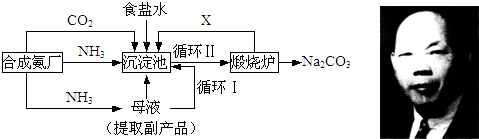
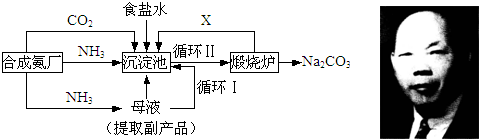
我国化学侯德榜(如图)改革国外的纯碱生产工艺,生产流程可简要表示如下:
沉淀池中四种盐在不同温度下的溶解度(g/100g水)表
| 温度溶解度盐 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | -① | - | - | - |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
请回答:
(1)沉淀池中反应温度控制在30℃~35℃,是因为若高于35℃,则______,若低于30℃,则______;为控制此温度范围,采取的加热方法为______.
(2)沉淀池中发生的化学反应方程式是______.
(3)副产品的一种用途为______,写出上述流程中X物质的分子式______.
(4)加料完毕后,继续保温30分钟,目的是______.静置后只析出NaHCO3晶体的原因是______.用蒸馏水洗涤NaHCO3晶体的目的是除去______杂质(以化学式表示).
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加______.
【答案】分析:(1)根据题中所给信息“35℃NH4HCO3会有分解”分析解答;根据影响反应速率的因素分析;要控制恒温,一般用水浴加热;
(2)根据联合制碱法的原料为氨气、二氧化碳和饱和氯化钠,反应式为NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3↓;
(3)主要的副产物为氯化铵,可以做化肥或电解液或焊药等;联合制碱法中二氧化碳是反应的原料同时也是反应的副产物,可以循环利用;
(4)分析溶解度数据,对比各物质的溶解度,根据溶解度越小越容易析出来分析.根据溶解平衡的知识分析剩余物的成分;
(5)检验氯离子的方法为用硝酸酸化的硝酸银来检验,若出现氯化银沉淀则说明有氯离子存在等知识点来解题.
解答:解:(1)根据题意“35℃NH4HCO3会有分解”,所以温度不能超过35℃;同时反应速度受温度影响,温度太低反应速率太慢,所以温度必须控制在一个合理范围内,使温度保持一个恒定,因为控制的温度在100℃以下,所以常用水浴加热来控制,
故答案为:NH4HCO3分解;反应速率降低;水浴加热;
(2)目前工业制碱方法有二:氨碱法和联合制碱法.题中方法由我们侯德邦所创,称为侯氏制碱法,也称为联合制碱法,反应方程式为:NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3↓,
故答案为:NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3↓;
(3)得到碳酸氢钠同时得到氯化铵,故副产物为氯化铵,氯化铵可用来制作化肥,也可用作焊药或电解液;煅烧炉中发生的反应是碳酸氢钠受热分解,生成纯碱、二氧化碳气体和水,所以X是二氧化碳,故答案为:化肥或电解液或焊药等;CO2;
(4)因为反应不是瞬间完成的,所以要保持一段时间,以使反应充分;由溶解度表可看出在30℃~35℃之间,碳酸氢钠的溶解度最小,所以析出的只能是碳酸氢钠;
因为未反应完的氯化钠、碳酸氢铵及生成的氯化铵会附着在碳酸氢钠晶体表面,所以要用蒸馏水进行洗涤,以便除去杂质;
故答案为:使反应充分进行;NaHCO3的溶解度最小;NaCl、NH4Cl、NH4HCO3;
(5)检验产品碳酸钠中是否含有氯化钠即检验是否含氯离子,可以用硝酸酸化的硝酸银,观察到若产生白色沉淀则说明有氯化钠存在,
故答案为:稀硝酸和硝酸银溶液.
点评:本题有一定难度,主要考查了学生运用溶解度有关知识分析解决纯碱制取过程中有关问题.联合制碱法的原料、反应式以及副产物的回收利用,如何提高原料的利用率、检验氯离子的方法是关键.
(2)根据联合制碱法的原料为氨气、二氧化碳和饱和氯化钠,反应式为NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3↓;
(3)主要的副产物为氯化铵,可以做化肥或电解液或焊药等;联合制碱法中二氧化碳是反应的原料同时也是反应的副产物,可以循环利用;
(4)分析溶解度数据,对比各物质的溶解度,根据溶解度越小越容易析出来分析.根据溶解平衡的知识分析剩余物的成分;
(5)检验氯离子的方法为用硝酸酸化的硝酸银来检验,若出现氯化银沉淀则说明有氯离子存在等知识点来解题.
解答:解:(1)根据题意“35℃NH4HCO3会有分解”,所以温度不能超过35℃;同时反应速度受温度影响,温度太低反应速率太慢,所以温度必须控制在一个合理范围内,使温度保持一个恒定,因为控制的温度在100℃以下,所以常用水浴加热来控制,
故答案为:NH4HCO3分解;反应速率降低;水浴加热;
(2)目前工业制碱方法有二:氨碱法和联合制碱法.题中方法由我们侯德邦所创,称为侯氏制碱法,也称为联合制碱法,反应方程式为:NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3↓,
故答案为:NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3↓;
(3)得到碳酸氢钠同时得到氯化铵,故副产物为氯化铵,氯化铵可用来制作化肥,也可用作焊药或电解液;煅烧炉中发生的反应是碳酸氢钠受热分解,生成纯碱、二氧化碳气体和水,所以X是二氧化碳,故答案为:化肥或电解液或焊药等;CO2;
(4)因为反应不是瞬间完成的,所以要保持一段时间,以使反应充分;由溶解度表可看出在30℃~35℃之间,碳酸氢钠的溶解度最小,所以析出的只能是碳酸氢钠;
因为未反应完的氯化钠、碳酸氢铵及生成的氯化铵会附着在碳酸氢钠晶体表面,所以要用蒸馏水进行洗涤,以便除去杂质;
故答案为:使反应充分进行;NaHCO3的溶解度最小;NaCl、NH4Cl、NH4HCO3;
(5)检验产品碳酸钠中是否含有氯化钠即检验是否含氯离子,可以用硝酸酸化的硝酸银,观察到若产生白色沉淀则说明有氯化钠存在,
故答案为:稀硝酸和硝酸银溶液.
点评:本题有一定难度,主要考查了学生运用溶解度有关知识分析解决纯碱制取过程中有关问题.联合制碱法的原料、反应式以及副产物的回收利用,如何提高原料的利用率、检验氯离子的方法是关键.

练习册系列答案
相关题目
我国化学侯德榜(如图)改革国外的纯碱生产工艺,生产流程可简要表示如下:
沉淀池中四种盐在不同温度下的溶解度(g/100g水)表
| 温度溶解度盐 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | -① | - | - | - |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
请回答:
(1)沉淀池中反应温度控制在30℃~35℃,是因为若高于35℃,则______,若低于30℃,则______;为控制此温度范围,采取的加热方法为______.
(2)沉淀池中发生的化学反应方程式是______.
(3)副产品的一种用途为______,写出上述流程中X物质的分子式______.
(4)加料完毕后,继续保温30分钟,目的是______.静置后只析出NaHCO3晶体的原因是______.用蒸馏水洗涤NaHCO3晶体的目的是除去______杂质(以化学式表示).
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加______.