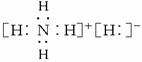题目内容
固体A的化学式为NH5,它的所有原子的最外层都符合相应的稀有气体原子电子层结构,该物质适当加热就分解成两种气体,试完成:
(1)固体A属于 晶体,它的电子式为 .
(2)A溶于水后溶液呈 性(填“酸”“碱”或“中”),其原因是(用化学方程式表示) .
(3)A与铜或铜的某些化合物在一定条件下可合成CuH,CuH是一种难溶物,它能在氯气中着火,还能与盐酸反应放出气体,请写出这两种反应的化学方程式 .
(1)固体A属于
(2)A溶于水后溶液呈
(3)A与铜或铜的某些化合物在一定条件下可合成CuH,CuH是一种难溶物,它能在氯气中着火,还能与盐酸反应放出气体,请写出这两种反应的化学方程式
分析:(1)根据A的性质可判断,A是氢化铵,属于离子化合物;
(2)A中的阴离子具有还原性,被水氧化生成氢气,所以溶于水后,和水发生反应生成氢气和一水合氨,溶液显碱性;
(3)氯气具有强氧化性,能氧化CuH,生成氯化铜和氯化氢.盐酸中的氢离子能氧化CuH的中氢生成氢气,同时还有氯化亚铜生成.
(2)A中的阴离子具有还原性,被水氧化生成氢气,所以溶于水后,和水发生反应生成氢气和一水合氨,溶液显碱性;
(3)氯气具有强氧化性,能氧化CuH,生成氯化铜和氯化氢.盐酸中的氢离子能氧化CuH的中氢生成氢气,同时还有氯化亚铜生成.
解答:解:(1)根据A的性质可判断,A是氢化铵,电子式为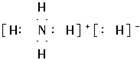 ,是离子化合物,形成离子晶体,
,是离子化合物,形成离子晶体,
故答案为:离子;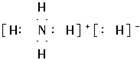 ;
;
(2)A中的阴离子具有还原性,被水氧化生成氢气,所以溶于水后,和水发生反应生成氢气和一水合氨,溶液显碱性,反应方程式为:NH4H+H2O═NH3?H2O+H2↑,
故答案为:碱;NH4H+H2O═NH3?H2O+H2↑;
(3)氯气具有强氧化性,能氧化CuH,生成氯化铜和氯化氢.盐酸中的氢离子能氧化CuH的中氢生成氢气,同时还有氯化亚铜生成,涉及方程式为:2CuH+3Cl2═2CuCl2+2HCl、CuH+HCl═CuCl+H2↑,
故答案为:2CuH+3Cl2═2CuCl2+2HCl、CuH+HCl═CuCl+H2↑.
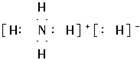 ,是离子化合物,形成离子晶体,
,是离子化合物,形成离子晶体,故答案为:离子;
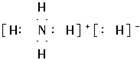 ;
;(2)A中的阴离子具有还原性,被水氧化生成氢气,所以溶于水后,和水发生反应生成氢气和一水合氨,溶液显碱性,反应方程式为:NH4H+H2O═NH3?H2O+H2↑,
故答案为:碱;NH4H+H2O═NH3?H2O+H2↑;
(3)氯气具有强氧化性,能氧化CuH,生成氯化铜和氯化氢.盐酸中的氢离子能氧化CuH的中氢生成氢气,同时还有氯化亚铜生成,涉及方程式为:2CuH+3Cl2═2CuCl2+2HCl、CuH+HCl═CuCl+H2↑,
故答案为:2CuH+3Cl2═2CuCl2+2HCl、CuH+HCl═CuCl+H2↑.
点评:本题以信息题形式,考查物质结构与性质、氧化还原反应、常用化学用语等,侧重考查学生对知识的迁移应用,是常见题型,难度中等.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目