题目内容
15. 已知反应:2N02 (红棕色)?N204 (无色)△H<0.将一定量的N02充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法正确的是( )
已知反应:2N02 (红棕色)?N204 (无色)△H<0.将一定量的N02充入注射器中后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法正确的是( )| A. | b点的操作是压缩注射器 | |
| B. | c点与a点相比,c(NO2)增大,c(N2O4)减小 | |
| C. | 若不忽略体系温度变化,且没有能量损失,则 r(b)>r(c) | |
| D. | d 点:v(正)>v(逆) |
分析 该反应是正反应气体体积减小的放热反应,压强增大平衡虽正向移动,但二氧化氮浓度增大,混合气体颜色变深,压强减小平衡逆向移动,但二氧化氮浓度减小,混合气体颜色变浅,据图分析,b点开始是压缩注射器的过程,气体颜色变深,透光率变小,c点后的拐点是拉伸注射器的过程,气体颜色变浅,透光率增大,据此分析.
解答 解:A、b点开始是压缩注射器的过程,气体颜色变深,透光率变小,故A正确;
B、c点是压缩注射器后的情况,二氧化氮和四氧化二氮的浓度都增大,故B错误;
C、b点开始是压缩注射器的过程,平衡正向移动,反应放热,导致r(b)<r(c),故C错误;
D、c点后的拐点是拉伸注射器的过程,d点是平衡向气体体积增大的逆向移动过程,所以v(逆)>v(正),故D错误;
故选A.
点评 本题通过图象和透光率考查了压强对平衡移动的影响,注意勒夏特列原理的应用,题目难度不大.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
5.短周期元素X、Y、Z的原子序数依次递增,三种元素的最外层电子数之和等于Z的原子序数.Y原子的最外层电子数是X原子内层电子数的3倍或者是Z原子最外层电子数的3倍.下列说法正确的是( )
| A. | X、Y元素能与氢形成分子式为H2XY2、H4X2Y2等弱酸 | |
| B. | 化合物ZY2中只含有离子键 | |
| C. | 工业上可用X单质置换ZY得到Z单质 | |
| D. | Y的氢化物的沸点比其下一周期的同族元素的氢化物的沸点低 |
3.下列各组元素中原子序数按由小到大顺序排列的是( )
| A. | Be、C、B | B. | Li、O、Cl | C. | Al、S、Si | D. | C、S、Mg |
20.下列各组物质中化学键的类型相同的是( )
| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O ? CO2 | ||
| C. | CaCl2 NaOH H2O | D. | NH3 H2O CO2 |
7.以下物质;①甲烷;②苯;③聚乙烯;④苯乙烯;⑤2-丁炔;⑥环己烷;⑦邻二甲苯.既能使KMnO4酸性溶液褪色,又能使溴水因发生化学反应而褪色的是( )
| A. | ④⑤ | B. | ④⑤⑦ | C. | ③④⑤ | D. | ③④⑤⑦ |
1.在一定条件下,RO3-与R-可发生反应:RO3-+5R-+6H+=3R2+3H2O,下列关于R元素的叙述中,正确的是( )
| A. | 元素R位于周期表中第ⅦA族 | |
| B. | RO3-中的R只能被还原 | |
| C. | R2在常温常压下一定是气体 | |
| D. | 若1 mol RO3-参与该反应,则转移电子的物质的量为6 mol |
2.下列离子方程式书写不正确的是( )
| A. | 少量铁粉加入稀盐酸中:Fe+2H+=Fe2++H2↑ | |
| B. | Ca(HCO3)2溶液与过量Ca(OH)2溶液反应:Ca2++HCO3-+OH-=CaCO3↓+H2O | |
| C. | NH4HCO3溶液和过量Ba(OH)2溶液共热:2HCO3-+2OH-+Ba2+=BaCO3↓+CO32-+2H2O | |
| D. | Na2S溶液中通入足量H2S:S2-+H2S=2HS- |
 ;取代反应
;取代反应 ,加聚反应
,加聚反应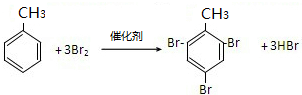 ;取代反应.
;取代反应.