题目内容
10.4g硫粉在氧气中完全燃烧生成二氧化硫,放出37kJ的热量,硫的燃烧热△H=-296kJ/mol;并写出热化学方程式S(s)+O2(g)=SO2(g)△H=-296kJ/mol.分析 根据燃烧热的含义结合热化学方程式的书写来回答,需要注意的有:物质的状态、反应热的数值与单位,反应热的数值与化学方程式前面的系数成正比.
解答 解:4g硫粉完全燃烧生成二氧化硫气体,放出37kJ的热量,所以32g硫粉完全燃烧生成二氧化硫气体,放出296kJ的热量,则热化学方程式为:S(s)+O2(g)═SO2(g)△H=-296kJ/mol,燃烧热是完全燃烧1mol物质生成最稳定的产物所放出的热量,所以硫的燃烧热为296 kJ/mol.
故答案为:-296kJ/mol;S(s)+O2(g)=SO2(g)△H=-296kJ/mol.
点评 本题考查了热化学方程式的书写,难度不大,注意掌握热化学方程式的书写规则.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.下列表达正确的是( )
| A. | HClO的电子式为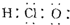 | |
| B. | H2S的电子式可表示为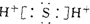 | |
| C. | 用电子式表示Na2O的形成过程为2Nax+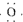 →2Na+ →2Na+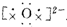 | |
| D. | MgCl2的电子式为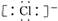 Mg2+ Mg2+ |
5.下列几个热化学方程式,△H能表示固体C或H2的燃烧热的是( )
| A. | C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol | B. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5kJ/mol | ||
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol | D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ/mol |
15.下列行为中符合安全要求的是( )
| A. | 节假日期间,在开阔的广场燃放烟花爆竹 | |
| B. | 进入煤矿井时,用火把照明 | |
| C. | 实验时,将水倒入浓硫酸配制稀硫酸 | |
| D. | 用点燃的火柴在液化气钢瓶口检验是否漏气 |
2.下列有机物,易溶于水的是( )
| A. | 溴乙烷 | B. | 乙醇 | C. | 油酸 | D. | 乙酸乙酯 |
19.下列反应中符合下图图象的是( )


| A. | N2(g)+3H2(g)?2NH3(g)△H=-Q1 kJ•mol-1 (Q1>0) | |
| B. | 2SO3(g)?2SO2(g)+O2(g)△H=+Q2 kJ•mol-1 (Q2>0) | |
| C. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-Q3 kJ•mol-1 (Q3>0) | |
| D. | H2(g)+CO(g)?C(s)+H2O(g)△H=+Q4 kJ•mol-1 (Q4>0) |
20.下列物质中的氢原子种类最多的是( )
| A. | 乙烷 | B. | 甲醇 | C. | 新戊烷 | D. | 环丙烷 |
 、
、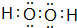 (用元素符号表示)
(用元素符号表示)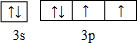 .
.