题目内容
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中通过以下反应制得
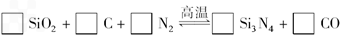
(1)配平上述反应的化学方程式(将化学计量数填在方框内);
(2)该反应中的氧化剂是________,其还原产物是________;
(3)该反应的平衡常数表达式为K=________;
(4)若知上述反应为放热反应,则其反应热ΔH________零(填“大于”“小于”或“等于”);升高温度,其平衡常数值________(填“增大”“减小”或“不变”);
(5)若使压强增大,则上述平衡向________反应方向移动(填“正”或“逆”);
(6)若已知CO生成速率为v(CO)=18 mol/(L·min),则N2消耗速率为v(N2)=________mol/(L·min).
(2)该反应中的氧化剂是________,其还原产物是________;
(3)该反应的平衡常数表达式为K=________;
(4)若知上述反应为放热反应,则其反应热ΔH________零(填“大于”“小于”或“等于”);升高温度,其平衡常数值________(填“增大”“减小”或“不变”);
(5)若使压强增大,则上述平衡向________反应方向移动(填“正”或“逆”);
(6)若已知CO生成速率为v(CO)=18 mol/(L·min),则N2消耗速率为v(N2)=________mol/(L·min).
(1)3 6 2 1 6
(2)N2;Si3N4
(3)
(4)小于;减小
(5)逆
(6)6
(2)N2;Si3N4
(3)

(4)小于;减小
(5)逆
(6)6

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
(14分)氮化硅(Si3N4)是一种新型陶瓷材料,它可由SiO2与过量焦炭在1300-1700oC的氮气流中反应制得3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)
(1)上述反应氧化剂是 ,已知该反应每转移1mole—,放出132.6kJ的热量,该方程式的∆H = 。
(2)能判断该反应(在体积不变的密闭容器中进行)已经达到平衡状态的是 。
A.焦炭的质量不再变化 B.N2和CO速率之比为1:3
C.生成6molCO同时消耗1mol Si3N4 D.混合气体的密度不再变化
(3)该反应的温度控制在1300-1700oC的原因是 。
(4)某温度下,测得该反应中N2和CO各个时刻的浓度如下,则0—20 min内N2的平均
反应速率 ,在平衡混合气体中CO的体积分数是 。
|
时间/min |
0 |
5 |
10 |
15 |
20 |
25 |
30 |
35 |
40 |
45 |
|
N2浓度 /mol·L-1 |
4.00 |
3.70 |
3.50 |
3.36 |
3.26 |
3.18 |
3.10 |
3.00 |
3.00 |
3.00 |
|
CO浓度 /mol·L-1 |
0.00 |
0.90 |
1.50 |
1.92 |
2.22 |
2.46 |
2.70 |
— |
— |
— |