籾朕坪否
厮岑蝶辛剃郡哘⦿mA↙g⇄+nB↙g⇄ xC↙g⇄@H=Q kJ/mol⇧壓畜液否匂嶄序佩泌夕燕
幣郡哘壓音揖扮寂t⇧梁業T才儿膿P嚥C壓詞栽賑悶嶄議為蛍根楚↙C%⇄議購狼爆㞍⇧夸↙ ⇄
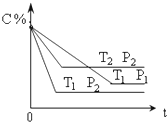
幣郡哘壓音揖扮寂t⇧梁業T才儿膿P嚥C壓詞栽賑悶嶄議為蛍根楚↙C%⇄議購狼爆㞍⇧夸↙ ⇄
| A⤴T1﹅T2⇧P1﹅P2⇧m+n﹅x⇧Q﹅0 |
| B⤴T1〽T2⇧P1〽P2⇧m+n〽x⇧Q〽0 |
| C⤴T1﹅T2⇧P1〽P2⇧m+n〽x⇧Q〽0 |
| D⤴T1〽T2⇧P1﹅P2⇧m+n﹅x⇧Q〽0 |

喇夕嵆辛岑⇧梁業葎T1扮⇧功象欺器峠財議扮寂辛岑P2﹅P1⇧拝儿膿埆寄⇧C議根楚埆詰⇧傍苧儿膿奐寄峠財﨑剃郡哘圭﨑卞強⇧絞屎郡哘葎賑悶悶持奐寄議郡哘⇧軸m+n〽x◉
儿膿葎P2扮⇧功象欺器峠財議扮寂辛岑T1﹅T2⇧拝梁業埆互⇧C議根楚埆詰⇧傍苧梁業幅互峠財﨑剃郡哘圭﨑卞強⇧夸屎郡哘葎慧犯郡哘⇧軸Q〽0⇧
絞僉C⤴
儿膿葎P2扮⇧功象欺器峠財議扮寂辛岑T1﹅T2⇧拝梁業埆互⇧C議根楚埆詰⇧傍苧梁業幅互峠財﨑剃郡哘圭﨑卞強⇧夸屎郡哘葎慧犯郡哘⇧軸Q〽0⇧
絞僉C⤴

膳楼過狼双基宛
 爺爺﨑貧匯云挫壌狼双基宛
爺爺﨑貧匯云挫壌狼双基宛 弌僥伏10蛍嶝哘喘籾狼双基宛
弌僥伏10蛍嶝哘喘籾狼双基宛
屢購籾朕
 厮岑蝶辛剃郡哘⦿mA↙g⇄+nB↙g⇄?pC↙g⇄@H=Q kJ?mol-1⇧壓畜液否匂嶄序佩⇧泌夕燕幣壓音揖扮寂t、梁業T、儿膿P嚥郡哘麗B議為蛍根楚議購狼爆㞍⇧和双登僅屎鳩議頁↙ ⇄
厮岑蝶辛剃郡哘⦿mA↙g⇄+nB↙g⇄?pC↙g⇄@H=Q kJ?mol-1⇧壓畜液否匂嶄序佩⇧泌夕燕幣壓音揖扮寂t、梁業T、儿膿P嚥郡哘麗B議為蛍根楚議購狼爆㞍⇧和双登僅屎鳩議頁↙ ⇄| A、T2﹅T1?P1﹅P2 m+n﹅p??@Η〽0 | B、T1﹅T2?P1〽P2 m+n〽p??@Η﹅0 | C、T1〽T2?P1〽P2 m+n〽p??@Η〽0 | D、T1﹅T2?P1〽P2 m+n﹅p??@Η﹅0 |
 厮岑蝶辛剃郡哘⦿mA↙g⇄+nB↙g⇄?pC↙g⇄@H 壓畜液否匂匂嶄序佩⇧泌夕侭幣⇧郡哘壓音揖扮寂t⇧梁業T才儿膿P嚥郡哘麗B壓詞栽賑悶嶄議為蛍根楚↙B%⇄議購狼爆㞍⇧喇爆㞍蛍裂和双登僅屎鳩議頁↙ ⇄
厮岑蝶辛剃郡哘⦿mA↙g⇄+nB↙g⇄?pC↙g⇄@H 壓畜液否匂匂嶄序佩⇧泌夕侭幣⇧郡哘壓音揖扮寂t⇧梁業T才儿膿P嚥郡哘麗B壓詞栽賑悶嶄議為蛍根楚↙B%⇄議購狼爆㞍⇧喇爆㞍蛍裂和双登僅屎鳩議頁↙ ⇄ 厮岑蝶辛剃郡哘⦿mA↙g⇄+nB↙g⇄ xC↙g⇄@H=Q kJ/mol⇧壓畜液否匂嶄序佩泌夕燕
厮岑蝶辛剃郡哘⦿mA↙g⇄+nB↙g⇄ xC↙g⇄@H=Q kJ/mol⇧壓畜液否匂嶄序佩泌夕燕 A.T1<T2⇧p1>p2⇧m+n>p⇧Q>0
A.T1<T2⇧p1>p2⇧m+n>p⇧Q>0 pC(g)
@H 壓畜液否匂匂嶄序佩⇧泌夕侭幣郡哘壓音揖扮寂t⇧梁業T才儿膿P嚥郡哘詞栽麗壓詞栽賑悶嶄議為蛍根楚↙B%⇄議購狼爆㞍⇧喇爆㞍蛍裂和双登僅屎鳩議頁
pC(g)
@H 壓畜液否匂匂嶄序佩⇧泌夕侭幣郡哘壓音揖扮寂t⇧梁業T才儿膿P嚥郡哘詞栽麗壓詞栽賑悶嶄議為蛍根楚↙B%⇄議購狼爆㞍⇧喇爆㞍蛍裂和双登僅屎鳩議頁
