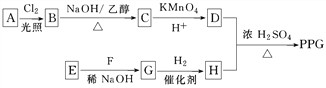
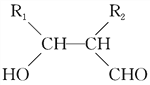
题目内容
【题目】二价铬不稳定,极易被氧化。醋酸亚铬水合物[Cr(CH3COO)2]2.2H2O,是一种深红色晶体,微溶于乙醇,不溶于冷水和乙醚。实验室以锌粒、CrCl3溶液、醋酸钠溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如图所示:

请回答下列问题:
(1)仪器A的名称是______,所盛装的试剂是_______。
(2)该实验中锌粒需过量,其原因除了与CrCl3充分反应得到CrCl2外,另一个作用是 ___________。
(3)写出C容器中制备醋酸亚铬水合物的离子方程式_______。
(4)仪器D的主要作用是_______。
(5)指出该装置的不足之处_______。
(6)Cr(OH)3的性质类似氢氧化铝,将CrCl3溶液蒸干灼烧,所得固体物质的化学式为_____。
(7)洗涤产品时,为了除去可溶性的杂质和水分,下列试剂正确使用的顺序是____(填序号)。
a.无水乙醇 b.冷的蒸馏水 c.乙醚
【答案】 分液漏斗 盐酸与CrCl3溶液 将CrCl2溶液压入锥形瓶C中,使其与醋酸钠溶液混合反应 2Cr2++4CH3COO—+2H2O =[Cr(CH3COO)2]2·2H20↓ 防止空气(O2)进入装置 实验开始时,没有将装置中的空气排尽 Cr2O3 b a c
【解析】(1)依据装置图形状和作用分析,仪器1为分液漏斗,根据题意,需要CrCl2溶液与醋酸钠溶液反应,因此在装置B中需要生成CrCl2溶液,且将溶液能够压入C中,因此分液漏斗中盛装稀盐酸和CrCl3溶液;故答案为:分液漏斗;盐酸与CrCl3溶液;
(2)实验中锌粒需过量,其中锌除了与CrCl3充分反应得到CrCl2外,还要与盐酸反应生成氢气,将CrCl2溶液压入锥形瓶C中,使其与醋酸钠溶液混合反应,故答案为:将CrCl2溶液压入锥形瓶C中,使其与醋酸钠溶液混合反应;
(3)C容器中制备醋酸亚铬水合物的离子方程式为2Cr2++4CH3COO—+2H2O =[Cr(CH3COO)2]2·2H2O↓,故答案为:2Cr2++4CH3COO—+2H2O =[Cr(CH3COO)2]2·2H2O↓;
(4) 二价铬不稳定,极易被氧化,仪器D可以防止空气(O2)进入装置,故答案为:防止空气(O2)进入装置;
(5) 二价铬不稳定,极易被氧化,实验开始时,无法将装置中的空气排尽,故答案为:实验开始时,没有将装置中的空气排尽;
(6)Cr(OH)3的性质类似氢氧化铝,将CrCl3溶液蒸干,促进CrCl3水解生成Cr(OH)3沉淀,进一步灼烧生成Cr2O3,故答案为:Cr2O3;
(7)洗涤产品时,为了除去可溶性的杂质和水分,由于醋酸亚铬水合物[Cr(CH3COO)2]2.2H2O微溶于乙醇,不溶于冷水和乙醚,需要先用冷水洗去可溶性的杂质,再用无水乙醇除去其中少量的水,最后用乙醚洗去附着的乙醇,故答案为:b a c。

【题目】已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:

溶质的物质的量浓度/mol·L-1 | 溶液的密度/g·cm-3 | |
硫酸 | c1 | ρ1 |
氨水 | c2 | ρ2 |
(1)表中硫酸的质量分数为__________(不写单位,用含c1、ρ1的代数式表示).
(2)物质的量浓度为c1mol·L-1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的物质的量浓度为__________mol·L-1.
(3)将物质的量浓度分别为c2mol·L-1和1/5c2mol·L-1的氨水等质量混合,所得溶液的密度__________(填“大于”、“小于”或“等于”,下同) ρ2 g·cm-3;所得溶液的物质的量浓度__________ 3/5c2mol·L-1(设混合后溶液的体积变化忽略不计).