题目内容
下列说法不正确的是
| A.氢氟酸能和玻璃的成分SiO2发生化学反应 |
B.根据SiO2+Na2CO3 Na2SiO3+CO2↑的反应,可推知硅酸的酸性比碳酸强 Na2SiO3+CO2↑的反应,可推知硅酸的酸性比碳酸强 |
| C.CO2气体通入到Na2SiO3溶液中可以制得硅酸 |
| D.原硅酸不稳定,易失去水分子成为硅酸 |
B
解析试题分析:A.氢氟酸能和玻璃的成分SiO2发生化学反应SiO2+4HF=SiF4↑+2H2O.正确。B.反应SiO2+Na2CO3 Na2SiO3+CO2↑是高沸点的酸制取低沸点的酸,这与溶液的酸性强弱无关。错误。C.由于酸性H2CO3>H2SiO3,所以CO2气体通入到Na2SiO3溶液中可以制得硅酸。正确。D.原硅酸不稳定,在室温下,在空气中易失去水分子成为硅酸。反应的方程式为H4SiO4= H2SiO3+H2O.错误。
Na2SiO3+CO2↑是高沸点的酸制取低沸点的酸,这与溶液的酸性强弱无关。错误。C.由于酸性H2CO3>H2SiO3,所以CO2气体通入到Na2SiO3溶液中可以制得硅酸。正确。D.原硅酸不稳定,在室温下,在空气中易失去水分子成为硅酸。反应的方程式为H4SiO4= H2SiO3+H2O.错误。
考点:考查物质的性质及强弱的比较的知识。

基于实验现象的推论,你认为合理的是( )
| 选项 | 实验现象 | 推论 |
| A | 乙烯气体可以使溴水褪色 | 乙烯发生取代反应 |
| B | 浓硫酸电导率比较低 | 硫酸浓度大时是弱电解质 |
| C | 氨气用于喷泉实验 | 氨气极易溶于水 |
| D | 硝酸溶液使pH试纸先变红后变白 | 硝酸酸性太强不能用pH试纸检测 |
可用如图装置制取(必要时可加热)、净化、收集的气体是( )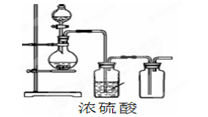
| A.铜和稀硝酸制一氧化氮 | B.氯化钠与浓硫酸制氯化氢 |
| C.锌和稀硫酸制氢气 | D.硫化亚铁与稀硫酸制硫化氢 |
实验室制取少量干燥的氨气涉及下列装置,其中正确的是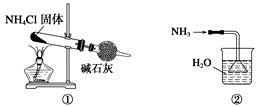
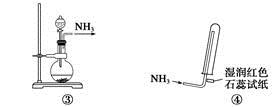
| A.①是氨气发生装置 | B.③是氨气发生装置 |
| C.②是氨气吸收装置 | D.④是氨气收集、检验装置 |
化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的特殊情况。下列反应中属于这种情况的是 ①过量的锌与18 mol·L-1的硫酸反应;②过量的氢气与少量氮气在催化剂存在下充分反应;③浓盐酸与过量的MnO2反应;④过量铜与浓硫酸反应;⑤过量稀硝酸与银反应;⑥过量稀硫酸与块状石灰石反应
| A.②③④⑥ | B.②③⑤ |
| C.①④⑤ | D.①②③④⑤⑥ |
5种常见物质X、Y、Z、E、F均含有同一元素M,已知Y是单质,Z是NO(一氧化氮),在一定条件下它们有如下转化关系,下列推断不合理的是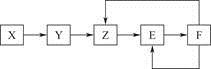
| A.X可能是一种 | B.M可能是金属 |
| C.E是一种有色气体 | D.X→Y可能是非氧化还原反应 |
某研究性学习小组做铜与浓硫酸反应实验时,发现试管底部有白色固体并夹杂有少量黑色物质。倒去试管中的浓硫酸,将剩余固体(含少量浓硫酸)倒入盛有少量水的烧杯中,发现所得溶液为蓝色,黑色固体未溶解。过滤、洗涤后,向黑色固体中加入过量浓硝酸,黑色固体溶解,溶液呈蓝色,所得溶液加BaCl2溶液后有白色沉淀生成。下列所得结论正确的是
| A.铜与浓硫酸反应所得白色固体不是CuSO4 |
| B.加BaCl2溶液后所得白色沉淀是BaSO3 |
| C.白色固体中夹杂的少量黑色物质可能是CuO |
| D.白色固体中夹杂的少量黑色物质中一定含有元素Cu和S |
下列制取硫酸铜的实验设计中,能体现“经济、高效、环保”精神的最佳方案是( )。
| A.铜与浓硫酸共热 |
| B.用铜片为阳极,石墨为阴极,电解稀硫酸 |
| C.先灼烧废铜屑生成氧化铜,然后再用浓硫酸溶解 |
| D.适当温度下,使铜片在持续通入空气的稀硫酸中溶解 |
烧瓶中放入铜片和稀硝酸,用酒精灯加热来制取较纯净的一氧化氮,反应开始后发现烧瓶中充满红棕色气体,这时的操作应是( )
| A.立即接收集容器,用向上排空气法收集 |
| B.待烧瓶中红棕色气体消失后,用向上排空气法收集 |
| C.待烧瓶中红棕色气体消失后,用排水法收集 |
| D.立即用排水法收集 |