题目内容
 根据右图提供的信息,下列所得结论不正确的是( )
根据右图提供的信息,下列所得结论不正确的是( )分析:根据反应物和生成物总能量的相对大小,来判断反应是吸热还是放热;根据物质能量的高低来判断物质的稳定性.
解答:解:A、因生成物总能量大于反应物的总能量,该反应为吸热反应,故A正确;
B、因能量守恒,必有其他形式的能量转化为化学能,故B正确;
C、因能量高的物质不稳定,能量低的物质稳定,而反应物的能量比生成物的能量低,所以反应物比生成物稳定,故C正确;
D、因反应是吸热还是放热与是否加热无关,故D错误;
故选:D.
B、因能量守恒,必有其他形式的能量转化为化学能,故B正确;
C、因能量高的物质不稳定,能量低的物质稳定,而反应物的能量比生成物的能量低,所以反应物比生成物稳定,故C正确;
D、因反应是吸热还是放热与是否加热无关,故D错误;
故选:D.
点评:化学反应同样遵循能量守恒定律,需要强调的是物质能量的高低来判断物质的稳定性有关.

练习册系列答案
相关题目
根据右图提供的信息,下列所得结论不正确的是( )
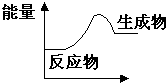

| A、该反应中化学能转化成了热能,为放热反应 | B、该反应一定有能量转化成了生成物的化学能 | C、该反应可以看成是其他形式的能量转化为化学能储存起来的过程 | D、反应物比生成物稳定 |
关于化学反应与能量的说法正确的是( )
| A.根据右图提供的信息,该反应是放热反应 |
| B.化学变化中的能量变化主要由化学键变化引起的 |
| C.化学反应中只伴随热量的变化 |
| D.CaCO3(s)==CaO(s)+CO2(g) ΔH="+178.5" KJ·mol-1的意义是表示1mol CaCO3完全分解生成1mol CaO和1mol CO2气体要放出178.5 KJ的热量 |

