题目内容
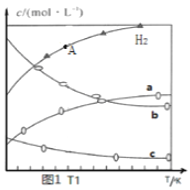
【题目】700℃时,H2(g)+CO2(g)![]() H2O(g)+CO(g).该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示.其中甲经2min达平衡时,v(H2O)为0.025mol/(Lmin),下列判断错误的是( )
H2O(g)+CO(g).该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,起始浓度如下表所示.其中甲经2min达平衡时,v(H2O)为0.025mol/(Lmin),下列判断错误的是( )
起始浓度 | 甲 | 乙 | 丙 |
c(H2)/mol/L | 0.10 | 0.20 | 0.20 |
c(CO2)/mol/L | 0.10 | 0.10 | 0.20 |
A. 平衡时,乙中CO2的转化率等于50%
B. 当反应平衡时,丙中c(CO2)是甲中的2倍
C. 温度升至800℃,上述反应平衡常数为25/16,则正反应为吸热反应
D. 其他条件不变,若起始时向容器乙中充入0.10mol/L H2和0.20 mol/LCO2,到达平衡时c (CO)与乙相同
【答案】AD
【解析】甲经2min达平衡时,v(H2O)为0.025mol/(Lmin),故△c(H2O)=0.025mol/(Lmin)×2min=0.05mol/L,则:
H2(g)+CO2(g)H2O(g)+CO(g)
开始(mol/L):0.1 0.1 0 0
转化(mol/L):0.05 0.05 0.05 0.05
平衡(mol/L):0.05 0.05 0.05 0.05
故该温度下平衡常数K=![]() =1,
=1,
A.令乙中CO2的浓度变化量为x,则:
H2(g)+CO2(g)H2O(g)+CO(g)
开始(mol/L):0.2 0.1 0 0
转化(mol/L): x x x x
平衡(mol/L):0.2-x 0.1-x x x
所以![]() =1,解得x=
=1,解得x=![]() ,故二氧化碳的转化率为
,故二氧化碳的转化率为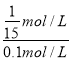 ×100%=66.7%,故A错误;B.反应前后气体的体积不变,恒温恒容下,甲、丙两容器内起始浓度n(H2):n(CO2)=1:1,甲、丙为等效平衡,平衡时二氧化碳的物质的量分数相同,丙中总物质的量为甲中的2倍,则反应平衡时,丙中c(CO2)是甲中的2倍,故B正确;C.温度升至800℃,上述反应平衡常数为
×100%=66.7%,故A错误;B.反应前后气体的体积不变,恒温恒容下,甲、丙两容器内起始浓度n(H2):n(CO2)=1:1,甲、丙为等效平衡,平衡时二氧化碳的物质的量分数相同,丙中总物质的量为甲中的2倍,则反应平衡时,丙中c(CO2)是甲中的2倍,故B正确;C.温度升至800℃,上述反应平衡常数为![]() ,大于700℃时的平衡常数K=1,则升高温度平衡向正反应方向移动,则正反应为吸热反应,故C正确;D.令平衡时CO的浓度为ymol/L,则:
,大于700℃时的平衡常数K=1,则升高温度平衡向正反应方向移动,则正反应为吸热反应,故C正确;D.令平衡时CO的浓度为ymol/L,则:
H2(g)+CO2(g)H2O(g)+CO(g)
开始(mol/L):0.1 0.2 0 0
转化(mol/L): y y y y
平衡(mol/L):0.1-y 0.2-y y y
则![]() =1,解得y=
=1,解得y=![]() ,而乙平衡时CO的浓度
,而乙平衡时CO的浓度![]() mol/L,故D错误;故:AD。
mol/L,故D错误;故:AD。

【题目】某小组同学通过“FeSO4被浓HNO3氧化”的实验,验证Fe2+的还原性。
实验一:验证Fe2+的还原性
实验操作 | 预期现象 | 实验现象 |
向盛有2 mL FeSO4溶液的试管中,滴入几滴浓硝酸,振荡 | 试管中产生红棕色气体,溶液变为黄色 | 试管中产生红棕色气体,溶液变为深棕色 |
(1)红棕色气体是_______。
(2)实验现象与预期不符,继续进行实验。
取深棕色溶液于试管中,滴加KSCN溶液,溶液变为红色,该现象说明_______。
实验二:探究溶液变为深棕色的原因
(资料与猜想)
查阅资料后猜想,可能是生成的NO2或NO与溶液中的Fe2+或Fe3+反应,而使溶液变为深棕色。
(实验与探究)
用下图所示装置进行实验(气密性已检验,尾气处理已略去)
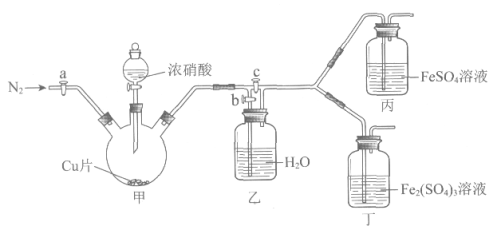
i. 关闭c,打开a和b,通入N2,一段时间后关闭a;
ii. 向甲中加入适量浓HNO3,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;
iii. 关闭b、打开c,更换丙、丁中的溶液(试剂不变);
iv. 继续向甲中加入浓HNO3,一段时间后观察到了与ii相同的实验现象。
(1)通入N2的目的是________。
(2)铜与浓硝酸反应的化学方程式是________。
(3)装置乙的作用是________。
(4)实验结论是________。
(反思与改进)
实验三:验证Fe2+的还原性
该小组同学依据实验二的结论改进了实验一,观察到了预期现象,其实验操作是________。