题目内容
9.维生素C是一种水溶性维生素(其水溶液呈酸性),结构如图所示.下列关于维生素C的叙述错误的是( )
| A. | 维生素C能使溴水褪色 | B. | 维生素C不能与碘单质反应 | ||
| C. | 维生素C可发生水解反应 | D. | 维生素C是较强的还原剂 |
分析 维生素C中含有羟基、酯基和碳碳双键,结合乙醇、乙酸乙酯和乙烯的性质推断有机物可能具有的性质,以此解答该题.
解答 解:A.有机物含有碳碳双键,可使溴水褪色,因发生加成反应,故A正确;
B.含有碳碳双键,可与碘反应,故B错误;
C.含有酯基,可发生水解反应,故C正确;
D.维生素C中的羟基、碳碳双键易被氧化,具有还原性,故D正确.
故选B.
点评 本题考查有机物的结构和性质,题目难度不大,注意有机物的含有的官能团的性质,此为解答该题的关键.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
19.已知Ksp(AgCl)=1.8×10-10 mol2•L-2,Ksp(AgI)=1.0×10-16 mol2•L-2.下列关于难溶物之间转化的说法中错误的是( )
| A. | AgCl不溶于水,不能转化为AgI | |
| B. | 两种难溶物的Ksp相差越大,难溶物就越容易转化为更难溶的物质 | |
| C. | AgI比AgCl更难溶于水,所以,AgCl可以转化为AgI | |
| D. | 常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低 1√1.8×10-11 mol•L-1 |
20.已知溴酸银的溶解是吸热过程,在不同温度下溴酸银溶解平衡曲线如图所示,下列说法正确的是( )
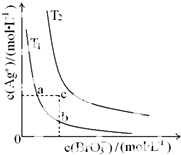

| A. | T1>T2 | |
| B. | 加入AgNO3固体,可使a点变到c点 | |
| C. | a点和b点的Ksp相等 | |
| D. | c点时,在T1、T2两个温度下均有固体析出 |
17.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 含1 mol H2SO4的浓硫酸与足量铜反应转移的电子总数为NA | |
| B. | 标准状况下,22.4 L O2 作氧化剂时转移电子数一定为4NA | |
| C. | 10 L 0.1 mol/L 的Na2CO3溶液中,Na+、CO32-总数为3NA | |
| D. | 通常状况下,4.2 g丙烯中所含碳氢键数目为0.6 NA |
4.下列各组物质中既具有相同的最简式,又不属于同分异构体和同系物的是( )
①聚乙烯和乙烯 ②甲醛和葡萄糖 ③淀粉和纤维素④蔗糖和麦芽糖 ⑤聚乙烯和聚氯乙烯.
①聚乙烯和乙烯 ②甲醛和葡萄糖 ③淀粉和纤维素④蔗糖和麦芽糖 ⑤聚乙烯和聚氯乙烯.
| A. | ①②④⑤ | B. | ①②③ | C. | ①③④⑤ | D. | ①②③⑤ |
14.COCl2(g)?CO(g)+Cl2(g)△H>0.当反应达到平衡时,下列措施:
①升温;②恒压通入惰性气体;③增加CO的浓度;④加催化剂;⑤减压;⑥恒容通入惰性气体.能提高COCl2转化率的是( )
①升温;②恒压通入惰性气体;③增加CO的浓度;④加催化剂;⑤减压;⑥恒容通入惰性气体.能提高COCl2转化率的是( )
| A. | ①④⑥ | B. | ①②⑤ | C. | ②③⑥ | D. | ③⑤⑥ |
1.欲证明一瓶无色液体是纯水,可靠的实验方法是( )(已知常温时,水的离子积为10-14,pH=7,NaCl溶解度为36g,加热时水易挥发)
| A. | 100℃时Kw=10-12 | |
| B. | 加热蒸干后无任何残留物 | |
| C. | 常温100g该液体中最多溶解NaCl固体36g | |
| D. | 常温下,阳离子总浓度c=10-7mol/L |
18.常温下某溶液中由水电离出的c(H+)与c(OH-)的乘积为10-20,该溶液可能是( )
| A. | pH等于4的NH4Cl溶液 | B. | pH等于4的H2SO4溶液 | ||
| C. | pH等于10的Na2CO3溶液 | D. | 一定浓度的NaCl溶液 |
