题目内容
【题目】在一定温度下,4L密闭容器内某一反应中气体M,气体N的物质的量随时间变化的曲线如图所示: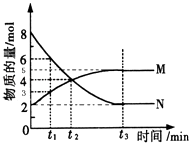
(1)比较t2时刻,正逆反应速率大小v正 v逆 . (填“>”、“=”、“<”)
(2)若t2=2min,计算反应开始至t2时刻,M的平均化学反应速率为:
(3)t3时刻化学反应达到平衡时反应物的转化率为
(4)如果升高温度则v逆(填增大、减小或不变).
【答案】
(1)>
(2)0.25mol/(L?min)
(3)75%
(4)增大
【解析】解:(1)根据图可知,在t2时刻气体N的物质的量在减小,M的物质的量在增加,所以反应在向正反应方向进行,此时v正>v逆 , 所以答案是:>;(2)根据v= ![]() 计算得M的平均化学反应速率为
计算得M的平均化学反应速率为 ![]() mol/(Lmin)=0.25mol/(Lmin),所以答案是:0.25mol/(Lmin);(3)根据图可知,从反应开始N的物质的量在减小,所以N为反应物,根据转化率=
mol/(Lmin)=0.25mol/(Lmin),所以答案是:0.25mol/(Lmin);(3)根据图可知,从反应开始N的物质的量在减小,所以N为反应物,根据转化率= ![]() ×100%计算得N的转化率为
×100%计算得N的转化率为 ![]() ×100%=75%,所以答案是:75%;(4)升高温度可逆反应中的正逆反应速率都增大,所以答案是:增大;
×100%=75%,所以答案是:75%;(4)升高温度可逆反应中的正逆反应速率都增大,所以答案是:增大;

练习册系列答案
相关题目