��Ŀ����
��10�֣����ӷ�Ӧ����ʽ��д����ע��д��ѧ����ʽ�����֣�
��1���������к��ռ��д���䷴Ӧ�����ӷ���ʽ��
��
��2����ϡ������ϴ���⣨Fe2O3������д���䷴Ӧ�����ӷ���ʽ��
��
��3���������ij���ʯ��ˮ���������̼����д���䷴Ӧ�����ӷ���ʽ��
��
��4��С�մ�������θ�ᣨ��Ҫ�����ᣩ���࣬��д���䷴Ӧ�����ӷ�
��ʽ�� ��
��5����������������������Һ������Ӧ����д���䷴Ӧ�����ӷ���ʽ��
��
��1���������к��ռ��д���䷴Ӧ�����ӷ���ʽ��
��
��2����ϡ������ϴ���⣨Fe2O3������д���䷴Ӧ�����ӷ���ʽ��
��
��3���������ij���ʯ��ˮ���������̼����д���䷴Ӧ�����ӷ���ʽ��
��
��4��С�մ�������θ�ᣨ��Ҫ�����ᣩ���࣬��д���䷴Ӧ�����ӷ�
��ʽ�� ��
��5����������������������Һ������Ӧ����д���䷴Ӧ�����ӷ���ʽ��
��
��10�֣�
(1) H++OH-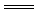 H2O��2�֣�
H2O��2�֣�
(2)Fe2O3+6H+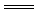 2Fe3++3H2O��2�֣�
2Fe3++3H2O��2�֣�
(3) CO2 + Ca2++2OH-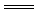 CaCO3��+H2O��2�֣�
CaCO3��+H2O��2�֣�
��4��HCO3-+H+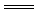 CO2�� + H2O��2�֣�
CO2�� + H2O��2�֣�
��5��2Al+2OH��+2H2O��2AlO2��+3H2����2�֣�
(1) H++OH-
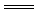 H2O��2�֣�
H2O��2�֣�(2)Fe2O3+6H+
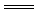 2Fe3++3H2O��2�֣�
2Fe3++3H2O��2�֣�(3) CO2 + Ca2++2OH-
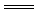 CaCO3��+H2O��2�֣�
CaCO3��+H2O��2�֣���4��HCO3-+H+
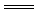 CO2�� + H2O��2�֣�
CO2�� + H2O��2�֣���5��2Al+2OH��+2H2O��2AlO2��+3H2����2�֣�
���ӷ�Ӧ����ʽ��д�ص��ǡ��𡱣���������ˮ��ǿ����ʲ�Ϊ��Ӧ�����ӣ�������ȷ����ɡ����ӵ�ʧ��ԭ�ӵ��غ�
��1�� H++OH-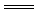 H2O
H2O
��2��Fe2O3+6H+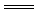 2Fe3++3H2O
2Fe3++3H2O
(3) CO2 + Ca2++2OH-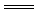 CaCO3��+H2O
CaCO3��+H2O
��4��HCO3-+H+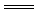 CO2�� + H2O
CO2�� + H2O
��5��2Al+2OH��+2H2O��2AlO2��+3H2��
��1�� H++OH-
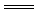 H2O
H2O��2��Fe2O3+6H+
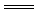 2Fe3++3H2O
2Fe3++3H2O(3) CO2 + Ca2++2OH-
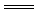 CaCO3��+H2O
CaCO3��+H2O��4��HCO3-+H+
 CO2�� + H2O
CO2�� + H2O��5��2Al+2OH��+2H2O��2AlO2��+3H2��

��ϰ��ϵ�д�
 53���ò�ϵ�д�
53���ò�ϵ�д�
�����Ŀ
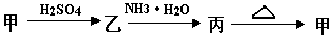
 2OH���� Cl2��+H2��
2OH���� Cl2��+H2��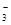 +5I
+5I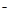 +3H2O=3I2+6OH
+3H2O=3I2+6OH NH3��+ 2H2O + CO32
NH3��+ 2H2O + CO32 2�����V���Ĺ�ϵ��ͼ��ͼ��AB�α�ʾ���Ⱥ����ӷ���ʽ�ǣ� ��
2�����V���Ĺ�ϵ��ͼ��ͼ��AB�α�ʾ���Ⱥ����ӷ���ʽ�ǣ� ��