题目内容
【题目】短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层有6个电子,Y是迄今发现的非金属性最强的元素,在周期表中Z位于I A族,W与X属于同一主族。下列说法正确的是 ( )
A.元素X、W的简单阴离子具有相同的电子层结构B.W的简单气态氢化物的热稳定性比Y的强
C.由Y、Z两种元素组成的化合物是离子化合物D.简单离子半径:r(X)<r(W)<r(Z)<r(Y)
【答案】C
【解析】
短周期主族元素 X、Y、Z、W 原子序数依次增大,X 原子的最外层有 6 个电子,X 为氧元素或硫元素,由于 X 的原子序数最小,则 X 是氧元素;Y 是迄今发现的非金属性最强的元素,Y 为氟元素;在周期表中 Z 位于ⅠA 族,Z 为钠元素,W 与 X 属于同一主族,W 为硫元素。
A. ![]() 有 2 个电子层,电子数分别为2、8,
有 2 个电子层,电子数分别为2、8,![]() 有 3 个电子层,电子数分别为2、8、8,A错误;
有 3 个电子层,电子数分别为2、8、8,A错误;
B. 非金属性:F>S,非金属性越强,氢化物越稳定,则热稳定性:HF>![]() ,B错误;
,B错误;
C. 钠和氟分别是活泼的金属和活泼的非金属,二者形成的化合物 NaF 为离子化合物,C正确;
D. 电子层数越多,离子半径越大,电子层数相同的情况下,核电荷数越大,离子半径越小,D错误;
答案选C。

 名校课堂系列答案
名校课堂系列答案【题目】短周期元素A,B,C在周期表中所处的位置如图所示。A,B,C三种元素原子的质子数之和为37,D元素原子的最外层电子数为次外层电子数的3倍。则下列说法正确的是
B | ||
A | C |
A.元素C形成的一种氧化物具有漂白性能使品红溶液和石蕊试液褪色
B.B,C两种元素的气态氢化物均能与它们的最高价氧化物对应的水化物发生反应,且反应类型相同
C.在高温下,元素A的氧化物可与它同主族的单质反应制取A的单质并生成![]()
D.四种元素形成的气态氢化物中,D元素形成的氢化物的稳定性最强,沸点也最高
【题目】研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH1=+489.0 kJ·mol-1
C(石墨)+CO2(g)=2CO(g) ΔH2=+172.5 kJ·mol-1
则CO还原Fe2O3的热化学方程式为___________________________
(2)某实验将CO2和H2充入一定体积的密闭容器中,在两种不同温度条件下反应:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1
测得CH3OH的物质的量随时间变化如图所示,回答问题:
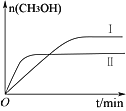
①该反应的平衡常数表达式K=_______________;
②曲线Ⅰ、Ⅱ对应的平衡常数大小关系为:KⅠ_________KⅡ(填“>”、“=”或“<”)。
③下列措施中能增大CO2转化率的是____________。(填序号)
A.升高温度 | B.充入He(g)使体系压强增大 |
C.将H2O(g)从体系中分离 | D.再充入一定量CO2 |
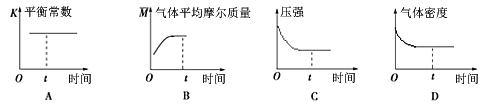
④下列图像正确且能表明在t时刻反应一定处于平衡状态的是__________。(填序号)