题目内容
(3分) 某金属X,为了确定其成分,进行一系列实验,实验过程和发生的现象如下图所示: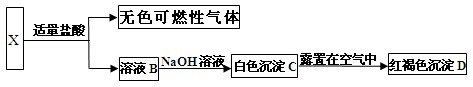
⑴写出金属X的化学式 。
⑵写出溶液B中溶质的化学式 。
⑶写出白色沉淀C转变为红褐色沉淀D的化学方程式 。(2分)
⑴ Fe 。⑵ FeCl2 。
⑶ 4Fe(OH)2+O2+2H2O=4Fe(OH)3。(2分)
解析

练习册系列答案
相关题目
题目内容
(3分) 某金属X,为了确定其成分,进行一系列实验,实验过程和发生的现象如下图所示:
⑴写出金属X的化学式 。
⑵写出溶液B中溶质的化学式 。
⑶写出白色沉淀C转变为红褐色沉淀D的化学方程式 。(2分)
⑴ Fe 。⑵ FeCl2 。
⑶ 4Fe(OH)2+O2+2H2O=4Fe(OH)3。(2分)
解析
