题目内容
【题目】将饱和FeCl3溶液滴入沸水中,煮沸一段时间后,当溶液变为红褐色时,停止加热,所得分散系。
(1)所得分散系与原FeCl3溶液是不同的分散系,其本质原因是 不同;要证明它们是不同的分散系,最简单的方法是利用 。
(2) 在制得的红褐色液体中逐滴加入少量稀硫酸,有什么现象:先 后 ,写出与现象有关的化学反应方程式_____________________
(3)如果FeCl3溶液中含有少量的NaCl,要除去NaCl得到纯净的FeCl3溶液,有下列方案:
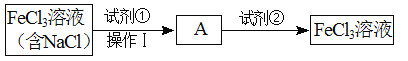
试剂②是 (填化学式);“操作Ⅰ”为 (填操作名称)。
【答案】(1)分散质颗粒直径大小 丁达尔效应
(2)浑浊 澄清 2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O
(3)HCl 过滤
【解析】
试题分析:(1)将饱和FeCl3溶液滴入沸水中,煮沸一段时间后,当溶液变为红褐色时,停止加热,所得分散系是胶体,氢氧化铁胶体和原FeCl3溶液是不同的分散系,其本质原因是分散质颗粒直径大小不同,胶体具有丁达尔效应,所以要证明它们是不同的分散系,最简单的方法是利用丁达尔效应。
(2)氢氧化铁胶体中逐滴加入少量电解质稀硫酸,会引起胶体聚沉,生成的氢氧化铁能和稀硫酸反应生成可溶性的硫酸铁和水,所以观察到的现象是先浑浊后澄清。与现象有关的化学反应方程式为2Fe(OH)3 + 3H2SO4 = Fe2(SO4)3+3H2O。
(3)FeCl3溶液中含有少量的NaCl,加入试剂①是氢氧化钠溶液,反应生成氢氧化铁沉淀,过滤得到A为Fe(OH)3,氢氧化铁沉淀加入试剂②为盐酸,氢氧化铁溶解生成氯化铁溶液,所以试剂②是HCl,操作Ⅰ为过滤。

练习册系列答案
相关题目