��Ŀ����
�������������Ű�ҹ��ֵ���������SO2����ɿ�������Ⱦ����Ҫԭ�������Ƽ�ѭ�����ɳ�ȥSO2��
��1���Ƽ�ѭ�����У�����ҺΪNa2SO3��Һ���÷�Ӧ�����ӷ���ʽ��________��
��2����֪H2SO3�ĵ��볣��ΪK1��1.54��10��2��K2��1.024��10��7��H2CO3�ĵ��볣��ΪK1��4.30��10��7��K2��5.60��10��11�������������Դ����������______������ţ���
A.CO32�� HSO3�� B. HCO3�� HSO3�� C. SO32�� HCO3�� D. H2SO3 HCO3��
��3������Һ����SO2�Ĺ����У�pH��n(SO32��):n(HSO3��)�仯��ϵ���±���
�ٸ����ϱ��ж�NaHSO3��Һ��_______�ԣ��Խ���ԭ��__________________________��
����NaHSO3��Һ������Ũ�ȹ�ϵ����ȷ����_______������ţ���
A��c(Na+)��2c(SO32-)+c(HSO3-)
B��c(Na+)��c(HSO3-)��c(H+)��c(SO32-)��c(OH-)
C��c(H2SO3)+ c(H+)��c(SO32-)+c(OH-)
D��c(Na+)+ c(H+)��2c(SO32-)+ c(HSO3-)+ c(OH-)
��4��������Һ��pH����ԼΪ6ʱ�����������۴�����ֱ���õ�pH��8������Һ��ѭ�����ã����ʾ��ͼ���£�
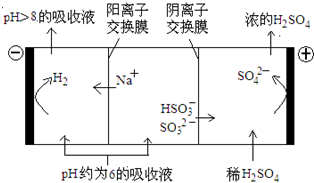
��д�������Ϸ����ĵ缫��Ӧʽ____________��
�ڵ��缫����1mol����ת��ʱ�������������Ϊ__________��
��1���Ƽ�ѭ�����У�����ҺΪNa2SO3��Һ���÷�Ӧ�����ӷ���ʽ��________��
��2����֪H2SO3�ĵ��볣��ΪK1��1.54��10��2��K2��1.024��10��7��H2CO3�ĵ��볣��ΪK1��4.30��10��7��K2��5.60��10��11�������������Դ����������______������ţ���
A.CO32�� HSO3�� B. HCO3�� HSO3�� C. SO32�� HCO3�� D. H2SO3 HCO3��
��3������Һ����SO2�Ĺ����У�pH��n(SO32��):n(HSO3��)�仯��ϵ���±���
| n(SO32��):n(HSO3��) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
�ٸ����ϱ��ж�NaHSO3��Һ��_______�ԣ��Խ���ԭ��__________________________��
����NaHSO3��Һ������Ũ�ȹ�ϵ����ȷ����_______������ţ���
A��c(Na+)��2c(SO32-)+c(HSO3-)
B��c(Na+)��c(HSO3-)��c(H+)��c(SO32-)��c(OH-)
C��c(H2SO3)+ c(H+)��c(SO32-)+c(OH-)
D��c(Na+)+ c(H+)��2c(SO32-)+ c(HSO3-)+ c(OH-)
��4��������Һ��pH����ԼΪ6ʱ�����������۴�����ֱ���õ�pH��8������Һ��ѭ�����ã����ʾ��ͼ���£�

��д�������Ϸ����ĵ缫��Ӧʽ____________��
�ڵ��缫����1mol����ת��ʱ�������������Ϊ__________��
��1��SO32����SO2��H2O��2HSO3����1�֣�
��2��BC��2�֣�ȫ�Ե�2�֣��д����÷֣�ѡ��ȫ��1�֣�
��3�����ᣨ1�֣�����������������Һ��HSO3�����ڵ���ƽ�⣺HSO3�� SO32����H����ˮ��ƽ��HSO3����H2O
SO32����H����ˮ��ƽ��HSO3����H2O H2SO3��OH����HSO3���ĵ���̶�ǿ��ˮ��̶ȣ�����Һ�����ԣ�2�֣���A��1�֣�
H2SO3��OH����HSO3���ĵ���̶�ǿ��ˮ��̶ȣ�����Һ�����ԣ�2�֣���A��1�֣�
��4����HSO3����H2O��2e����SO42����3H����2�֣���1g��1�֣�
��2��BC��2�֣�ȫ�Ե�2�֣��д����÷֣�ѡ��ȫ��1�֣�
��3�����ᣨ1�֣�����������������Һ��HSO3�����ڵ���ƽ�⣺HSO3��
 SO32����H����ˮ��ƽ��HSO3����H2O
SO32����H����ˮ��ƽ��HSO3����H2O H2SO3��OH����HSO3���ĵ���̶�ǿ��ˮ��̶ȣ�����Һ�����ԣ�2�֣���A��1�֣�
H2SO3��OH����HSO3���ĵ���̶�ǿ��ˮ��̶ȣ�����Һ�����ԣ�2�֣���A��1�֣���4����HSO3����H2O��2e����SO42����3H����2�֣���1g��1�֣�
�����������1���������Ƕ�Ԫ���ᣬ������������SO2ת��Ϊ��ʽ�Σ������Ƽ�ѭ�����У�����ҺΪNa2SO3��Һʱ��Ӧ�����ӷ���ʽΪSO32����SO2��H2O��2HSO3����
��2������ĵ��볣��Խ������Խǿ�������H2SO3�ĵ��볣��ΪK1��1.54��10��2��K2��1.024��10��7��H2CO3�ĵ��볣��ΪK1��4.30��10��7��K2��5.60��10��11��֪������ǿ��˳����H2SO3��H2CO3��HSO3����HCO3�������ݽ�ǿ�����Ʊ����������֪��CO32����HSO3����Ӧ����HCO3����SO32�������ܴ������棻H2SO3��HCO3����Ӧ����CO2��HSO3�������ܴ������档��HCO3����HSO3����SO32����HCO3�������Դ������棬��ѡBC��
��3��������SO32��ֻ��ˮ�⣬��Һ�Լ��ԣ����Ը���n(SO32��):n(HSO3��)��1:91ʱ��Һ�����Կ�֪��NaHSO3��Һ�����ԡ�����������������������Һ��HSO3�����ڵ���ƽ�⣺HSO3��
 SO32����H����ˮ��ƽ��HSO3����H2O
SO32����H����ˮ��ƽ��HSO3����H2O H2SO3��OH����HSO3���ĵ���̶�ǿ��ˮ��̶ȣ�����Һ�����ԡ�
H2SO3��OH����HSO3���ĵ���̶�ǿ��ˮ��̶ȣ�����Һ�����ԡ��ڸ��������غ��֪��c(Na+)��c(SO32-)+c(HSO3-)+ c(H2SO3)��A����ȷ��B������HSO3���ĵ���̶�ǿ��ˮ��̶ȣ��Ҿ��Ǻ����ģ�������Һ��c(Na+)��c(HSO3-)��c(H+)��c(SO32-)��c(OH-)��B��ȷ��C�����ݵ���غ��֪c(Na+)+ c(H+)��2c(SO32-)+ c(HSO3-)+ c(OH-)�������غ��֪c(Na+)��c(SO32-)+c(HSO3-)+ c(H2SO3)����Һ��c(H2SO3)+ c(H+)��c(SO32-)+c(OH-)��C��ȷ��D�����ϵ���غ�c(Na+)+ c(H+)��2c(SO32-)+ c(HSO3-)+ c(OH-)��D��ȷ����ѡA��
��4���ٵ������������Դ������������ʧȥ���ӣ�����������Ӧ������װ�ÿ�֪�������������ɣ�������Һ��pH��6����Һ����Ҫ����HSO3-���ڣ�����������Ҫ��HSO3-�ŵ磬��������Ϸ����ĵ缫��ӦʽΪHSO3����H2O��2e����SO42����3H����
�ڵ����������õ����裬�����װ�ÿ��ж���������Һ�е������ӷŵ������������缫��ӦʽΪ2H����2e����H2�������缫����1mol����ת��ʱ�����õ�0.5mol�����������������������Ϊ0.5mol��2g/mol��1g��

��ϰ��ϵ�д�
 ��ĩ1�����ʽ���������ϵ�д�
��ĩ1�����ʽ���������ϵ�д�
�����Ŀ