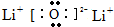题目内容
根据周期表对角线规则,金属铍与铝的单质及其化合物性质相似,又已知氯化铝的熔沸点较低,易升华。回答下列问题。(1)写出铍与氢氧化钠反应的离子方程式
_________________________________________________________________。
(2)氢氧化铍与氢氧化镁可用_______________鉴别,其离子方程式是____________________。氯化铍属于化合物______________(填“离子”或“共价”)。
(3)锂和镁据对角线规则,性质也相似。锂在空气中燃烧主要产物的电子式是___________,同时还有少量的___________生成。
解析:根据铍与铝的性质相似,单质能与氢氧化钠反应生成铍酸钠和氢气,氢氧化物有两性,与氢氧化钠反应生成铍酸钠和水,可用氢氧化钠溶液鉴别氢氧化镁和氢氧化铍。根据氯化铝的性质可知,它为分子晶体。镁能和空气中的氧气、氮气反应,锂的性质与镁类似,会发生与镁一样的反应和产物。
答案:(1)Be+2OH-====![]() +H2↑
+H2↑
(2)NaOH;Be(OH)2+2 OH-====![]() +2H2O 共价
+2H2O 共价
(3)Li+[![]() ]2-Li+ Li3N
]2-Li+ Li3N

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案
相关题目