题目内容
将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入0.5 L密闭容器内,550℃时,在催化剂作用下发生反应:2SO2(g)+O2(g) 2SO3(g)(正反应放热)。测得n(O2)随时间的变化如下表
2SO3(g)(正反应放热)。测得n(O2)随时间的变化如下表
|
时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
|
n(O2)/mol |
0.7 |
0.4 |
0.3 |
x |
x |
x |
反应达到5s后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了22.4L(此体积为标准状况下的体积);再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(此体积为标准状况下的体积)。
请回答下列问题:
(1)用O2表示从0~1s内该反应的平均反应速率为 ;
(2)O2的平衡浓度c(O2)= ;
(3)4s时,SO2的生成速率____________(填“大于”、“小于”或“等于”)O2的消耗速率。
(4)求该反应达到平衡时SO2的转化率是____________(用百分数表示)。
(5)若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀____________克(计算结果保留一位小数)。
(每空2分、共10分)(1)0.6mol·L-1·s-1(2)0. 5mol·L-1
(3)大于 (4)90% (5)10.5
【解析】
试题分析:(1)根据表中数据可知,从0~1s内氧气的物质的量减少了0.7mol-0.4mol=0.3mol,所以用O2表示从0~1s内该反应的平均反应速率为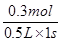 =0.6mol·L-1·s-1。
=0.6mol·L-1·s-1。
(2)反应达到5s后,将容器中的混合气体通过过量NaOH溶液,气体体积减少了22.4L(此体积为标准状况下的体积),这说明容器中SO2和三氧化硫的总的物质的量是22.4L÷22.4L/mol=1mol。因此根据原子守恒可知,反应前通入的SO2是1mol。再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(此体积为标准状况下的体积),所以属于氧气的物质的量是5.6L÷22.4L/mol=0.25mol,所以O2的平衡浓度c(O2)=0.25mol÷0.5L=0.5mol/L。
(3)4s时,反应达到平衡状态,则根据方程式可知SO2的生成速率大于O2的消耗速率。
(4)平衡时消耗氧气是0.7mol-0.25mol=0.45mol,则根据方程式可知,消耗SO2的物质的量是0.45mol×2=0.9mol,所以SO2的平衡转化率是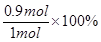 =90%。
=90%。
(5)平衡时生成三氧化硫是0.9mol,若将平衡混合气体的5%通入过量的BaCl2溶液,生成沉淀的质量是0.9mol×5%×233g/mol=10.5g。
考点:考查可逆反应的有关计算
点评:该题是高考中的常见题型,属于中等难度试题的考查。试题设计新颖,基础性强。在注重对学生基础知识巩固和训练的同时,侧重对学生分析、归纳和总结问题的能力,有利于培养学生的逻辑推理能力和规范答题能力。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案