题目内容
已知可逆反应:2SO2(g)+O2(g)?2SO3(g),下列关于此反应的说法中错误的是( )
分析:A.根据压强越大,反应速率越大;
B.根据反应反应中断裂旧化学键所需要吸收的能量小于形成新化学键释放的能量;
C.根据可逆反应不能完全进行到底;
D.根据反应达到平衡状态时,正逆反应速率相等.
B.根据反应反应中断裂旧化学键所需要吸收的能量小于形成新化学键释放的能量;
C.根据可逆反应不能完全进行到底;
D.根据反应达到平衡状态时,正逆反应速率相等.
解答:解:A.加压,反应物的浓度增大,反应速率变大,故A正确;
B.该反应为放热反应,所以形成新化学键释放的能量大于断裂旧化学键所需要吸收的能量,故B正确;
C.将2molSO2和1molO2混合进行反应,反应完成时生成小于2molSO3,故C错误;
D.单位时间内生成2molSO3,同时生成1molO2说明说明正逆反应速率相等,反应达到平衡状态,故D正确;
故选C.
B.该反应为放热反应,所以形成新化学键释放的能量大于断裂旧化学键所需要吸收的能量,故B正确;
C.将2molSO2和1molO2混合进行反应,反应完成时生成小于2molSO3,故C错误;
D.单位时间内生成2molSO3,同时生成1molO2说明说明正逆反应速率相等,反应达到平衡状态,故D正确;
故选C.
点评:本题考查了化学反应速率、平衡的因素,可逆反应的限度,反应中的热效应,难度不大,注意知识的运用.

练习册系列答案
相关题目
 4C(g)
△H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)
4C(g)
△H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)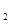 (g)
(g) 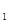 与K
与K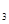 的平衡常数K=19。在该温度下的体积
的平衡常数K=19。在该温度下的体积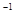 c0(O
c0(O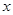 kJ·mol
kJ·mol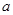 +b>
+b>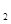 (g)的平衡常数为K1;H
(g)的平衡常数为K1;H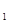 与K
与K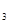 的平衡常数K=19。在该温度下的体积
的平衡常数K=19。在该温度下的体积 容包括:化学平衡、电离平衡、水解平衡和
容包括:化学平衡、电离平衡、水解平衡和 4C(g) △H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)
4C(g) △H>0达到平衡时,c(A)=2mol/L,c(B)=7mol/L,c(c)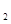 (g)
(g) 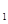 与K
与K 的平衡常数K=19。在该温度下的体积
的平衡常数K=19。在该温度下的体积 c0(O
c0(O
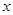 kJ·mol
kJ·mol +b>
+b>