题目内容
南海某小岛上,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验,结果显示水的硬度为280(属于硬水),主要含钙离子、镁离子、氯离子和硫酸根离子。请回答下列问题。
(1)该泉水属于 硬水(填写“暂时”或“永久”)。
(2)若要除去Ca2+、Mg2+可以往水中加入石灰和纯碱,试剂加入时的先后次序是 ,原因是 。
(3)目前常用阴、阳离子交换树脂来进行硬水的软化,如水中的Ca2+、Mg2+可与交换树脂中的 交换。当阴离子交换树脂失效后可放入 溶液中再生。
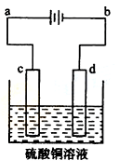
(4)岛上还可以用海水淡化来获得淡水。右边是海水利用电渗析法获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。请分析下列问题:
①阳离子交换膜是指 (填A或B);
②写出通电后阳极区的电极反应式: 。
(1)永久(2分)
(2)先加石灰,后加纯碱(2分);过量的钙离子可通过纯碱使之沉淀(3分)
(3)H+(2分);强碱(2分)
(4)①B(2分) ②2Cl――2e-=Cl2↑(2分)
解析试题分析:(1)岛上的山泉水是永久硬水,(2)先加Ca(OH)2使Mg2+沉淀,再加Na2CO3可以除去过量的Ca2+;(3)阳离子树脂交换阳离子H+,阴离子交换阴离子OH-所以失效后在强碱中再生;(4)在电解池中,阴极H+放电,留下OH-,阳离子Ca2+、Mg2+移向阴极,形成沉淀,阳离子交换膜是指B,阳极Cl-失电子发生氧化反应。
考点:考查硬水处理、离子的性质、电解池原理

迄今为止,由化学能转变的热能或电能仍然是人类使用的主要的能源。
I.请仔细观察下列两种电池的构造示意图,完成下列问题:
(1)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素分析其原因是 。
(2)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应式为 。
Ⅱ.下面是一个将化学能与电能相互转化的装置。回答下列问题:
(1)写出通入O2一极的电极反应方程式为 。
(2)a电极是 极,能否写出其电极反应方程式 (填“能”或“不能”),若“能”写出其电极反应方程式,若“不能”说明其理由 。
(3)下列说法不正确的是( )
| A.此装置用于电镀铜时,电解一段时间,硫酸铜溶液的浓度不变 |
| B.U型管中,OH—在a极放电 |
| C.若a为纯净金属,b为粗制金属,该装置可用于粗制金属的精炼 |
| D.电子经导线流入b电极 |

下列实验方案不合理的是( )
| A.除去乙烷中含有的乙烯:将气体通入溴水中,洗气 |
| B.检验蔗糖是否水解:取1mL 20%的蔗糖溶液,加3~5滴稀硫酸。水浴加热5min后取少量溶液,加氢氧化钠溶液调溶液pH至碱性,再加入少量新制备的Cu(OH)2,加热3~5 min,观察实验现象 |
| C.除去乙酸乙酯中的乙酸:加入浓硫酸和乙醇,加热 |
| D.鉴别己烯和苯:将溴的四氯化碳溶液分别滴加到少量己烯和苯中 |




 沉淀完全,而在pH≥3.2时
沉淀完全,而在pH≥3.2时

 为d,则此时的铬酸钾的转化率为 。
为d,则此时的铬酸钾的转化率为 。