题目内容
【题目】某些电镀厂的酸性废水中常含有一定量的CrO42-和Cr2O72-,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法,该法的工艺流程为:
![]()
其中第①步存在平衡步存在平衡:2CrO42-(黄色)+2H+![]() Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)若平衡体系的pH=12,该溶液显________色。
(2)写出第③步的离子反应方程式:__________。
(3)第②步中,用6mol的FeSO4·7H2O可还原________molCr2O72-离子。
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s) ![]() Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至_______。
方法2:电解法:该法用Fe做电极电解含Cr2O72-的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(5)写出阳极的电极反应式___________________。
(6)在阴极附近溶液pH升高的原因是(用电极反应解释)__________________________
(7)用电镀法在铁制品上镀上一层锌,则阴极上的电极反应式为____________。
【答案】(1)黄;
(2)Cr3++3OH-=Cr(OH)3↓;
(3)1;(4)5;
(5)Fe-2e-=Fe2+;
(6)2H++2e-=H2↑;
(7)Zn2++2e-=Zn。
【解析】
试题分析:(1)c(H+)减小,平衡2CrO42-(黄色)+2H+![]() Cr2O72-(橙色)+H2O左移,溶液呈黄色,故答案为:黄;
Cr2O72-(橙色)+H2O左移,溶液呈黄色,故答案为:黄;
(2)第③步是沉淀铬离子的反应,离子反应方程式为Cr3++3OH-=Cr(OH)3↓,故答案为:Cr3++3OH-=Cr(OH)3↓;
(3)6mol亚铁离子被氧化为+3价,失去6mol电子,Cr2O72-离子中铬元素化合价从+6价降低到+3价,应该得到6mol电子,所以6mol的FeSO4·7H2O可还原1mol Cr2O72-离子,故答案为:1;
(4)Cr(OH)3的溶度积Ksp=c(Cr3+)c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,则需c(OH-)=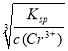 =
=![]() =10-9mol/L,所以c(H+)=10-5mol/L,即pH=5,故答案为:5;
=10-9mol/L,所以c(H+)=10-5mol/L,即pH=5,故答案为:5;
(5)在电解法除铬中,铁作阳极,阳极反应为Fe-2e-═Fe2+,以提供还原剂Fe2+,故答案为:Fe-2e-=Fe2+;
(6)在阴极附近溶液pH升高的原因是水电离产生的H+放电生成H2:2H++2e-═H2↑;故答案为:2H++2e-=H2↑;
(7)用电镀法在铁制品上镀上一层锌,阴极上的电极反应式为Zn2++2e-=Zn,故答案为:Zn2++2e-=Zn。

 阅读快车系列答案
阅读快车系列答案