题目内容
(2013?潍坊模拟)下列说法中,不正确的是( )
分析:A、根据每层最多容纳的电子数为2n2个,最外层电子数不超过8个,倒数第二层不超过18个等来分析;
B、非金属性越强,与氢气化合越容易;
C、由质量数=质子数+中子数来计算;
D、根据含有离子键的化合物一定是离子化合物并利用常见物质中的化学键来解答.
B、非金属性越强,与氢气化合越容易;
C、由质量数=质子数+中子数来计算;
D、根据含有离子键的化合物一定是离子化合物并利用常见物质中的化学键来解答.
解答:解:A、因第一层最多排2个电子,第二层最多排8个电子,第三层最多排布18个电子,且在每层最多容纳的电子数为2n2个时,同时符合最外层电子数不超过8个,倒数第二层不超过18个,显然原子最外层电子数比次外层电子数多的元素一定位于第二周期,故A正确;
B、从氟到碘非金属性逐渐减弱,则与氢气发生化合反应越来越难,故B正确;
C、14C的中子数为14-6=8,14N的中子数14-7=7,中子数不同,故C错误;
D、含有离子键的化合物一定是离子化合物,但离子化合物中可以含有共价键,如NaOH等,故D正确;
故选C.
B、从氟到碘非金属性逐渐减弱,则与氢气发生化合反应越来越难,故B正确;
C、14C的中子数为14-6=8,14N的中子数14-7=7,中子数不同,故C错误;
D、含有离子键的化合物一定是离子化合物,但离子化合物中可以含有共价键,如NaOH等,故D正确;
故选C.
点评:本题考查知识点较多,学生应熟悉原子的电子排布、非金属性的比较、物质中的化学键、原子的构成等知识来解答,本题中A是学生解答的难点.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
 (2013?潍坊模拟)如图,“低碳生活”是指生活作息时所耗用能量要减少,从而降低碳特别是二氧化碳的排放.下列行为不利于低碳生活的是( )
(2013?潍坊模拟)如图,“低碳生活”是指生活作息时所耗用能量要减少,从而降低碳特别是二氧化碳的排放.下列行为不利于低碳生活的是( )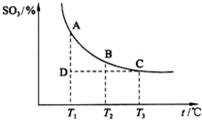 (2013?潍坊模拟)如图,研究碳、氮、硫的氧化物的性质对化工生产和环境保护有重要意义.
(2013?潍坊模拟)如图,研究碳、氮、硫的氧化物的性质对化工生产和环境保护有重要意义.